Vous êtes ici
Alzheimer : les espoirs de la piste sanguine
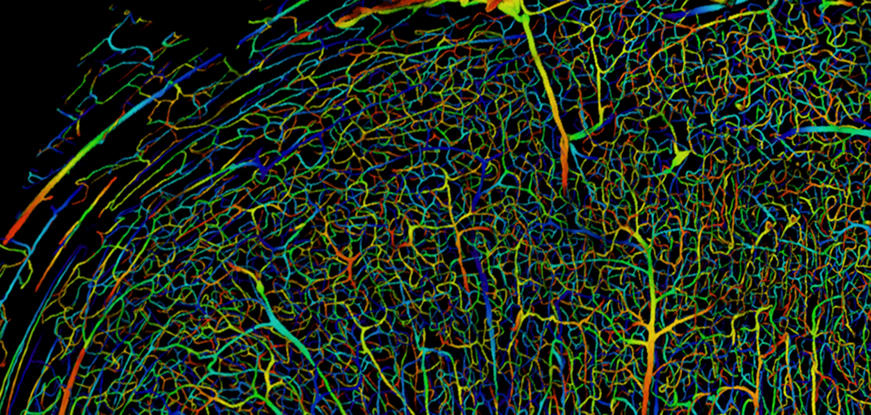
Avec 900 000 personnes atteintes aujourd’hui en France, la maladie d’Alzheimer est la plus fréquente des maladies neurodégénératives. Bien que, depuis plus de dix ans, plusieurs pistes aient été explorées1, aucun traitement n’existe à l’heure actuelle pour guérir la maladie ni même en ralentir l’évolution. Devant cette impasse, des voies de recherches alternatives et parfois inattendues émergent. Parmi elles : la mise en cause de dysfonctionnements précoces au niveau de la circulation sanguine du cerveau. Cette hypothèse soutenue par l’équipe du projet BrainMicroFlow2 pointe précisément le rôle des capillaires qui irriguent le cerveau, un réseau d’environ mille milliards de vaisseaux sanguins, chacun dix fois plus fins que le diamètre d’un cheveu, et qui viendraient à s’obstruer par milliers dès le stade initial de la maladie.
Une origine vasculaire de la maladie ?
« Notre hypothèse a de quoi surprendre puisque, depuis longtemps, la maladie d’Alzheimer est classée parmi les maladies neurodégénératives sans origine vasculaire », commente Sylvie Lorthois, chercheuse à l’Institut de mécanique des fluides de Toulouse3 et porteuse du projet. Une hypothèse pourtant prise très au sérieux : le projet s’est vu attribuer en 2014 le prestigieux prix du Conseil européen de la recherche (ERC), qui récompense des travaux de recherche de pointe, originaux et porteurs d’idées en rupture. Avec à la clé 2 millions d’euros sur cinq ans, de quoi donner un véritable coup d’accélérateur aux travaux initiés depuis plusieurs années par la chercheuse.
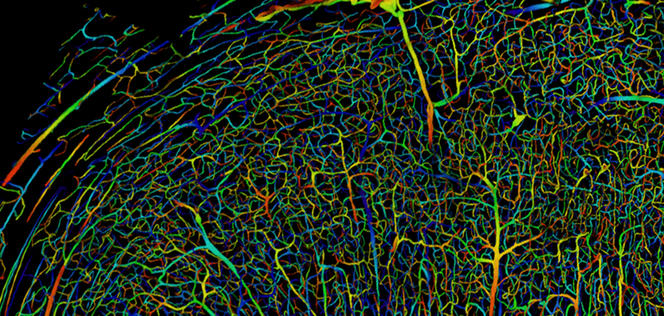
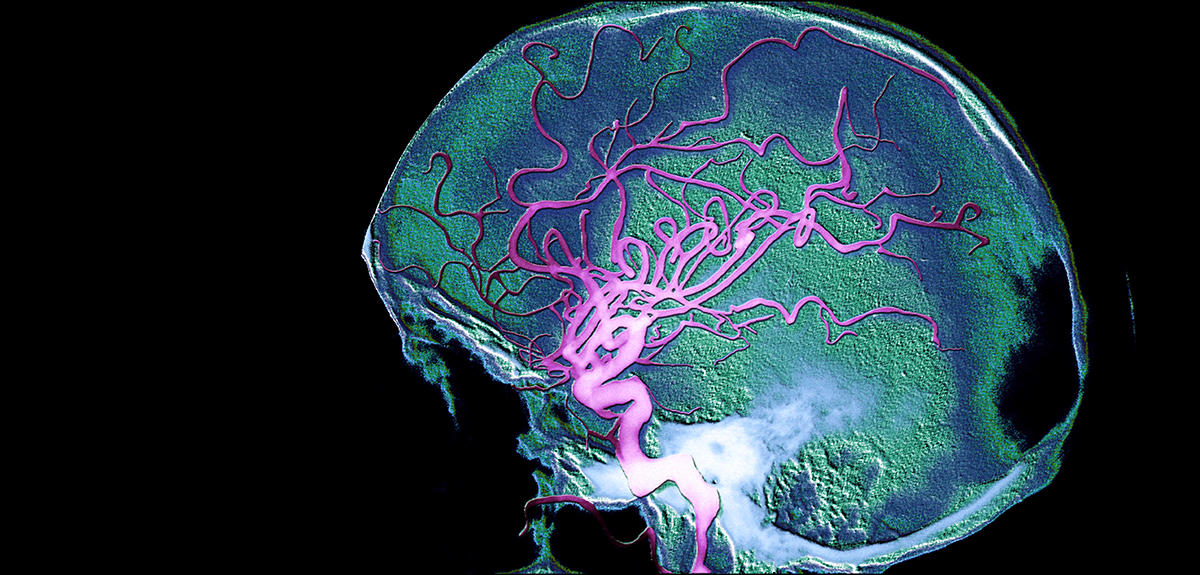
« Actuellement, on estime à environ 30 % la baisse du débit sanguin cérébral chez les patients à un stade avancé de la maladie, soit une baisse équivalente à ce que nous pouvons expérimenter lorsque, assis au sol, nous nous relevons d’un seul coup, explique Sylvie Lorthois. Ce ralentissement de l’écoulement sanguin est connu depuis longtemps, mais il était considéré jusqu’à présent comme une conséquence de la mort des neurones observée dans la maladie d’Alzheimer, et non comme une des causes possibles. »
Seulement voilà : l’IRM, la technique d’imagerie médicale la plus utilisée pour observer le cerveau, ne permet pas de voir à l’échelle de ces réseaux de capillaires.
Pour étudier leur rôle dans la survenue de la maladie d’Alzheimer, les chercheurs ont donc misé sur la modélisation. Et leurs modèles de mécanique des fluides, qui simulent la circulation sanguine dans ces réseaux ultrafins, constituent une vraie première. Ils reproduisent en laboratoire l’écoulement du sang à travers des réseaux de canaux en silicone d’environ 10 micromètres de diamètre4, l’équivalent du diamètre réel des capillaires.
« Concrètement, nous faisons circuler des globules rouges à l’intérieur d’un réseau de canaux qui peuvent être organisés selon différentes géométries, en nid d’abeille par exemple. Grâce à un microscope équipé d’une caméra rapide capable d’acquérir plusieurs milliers d’images par seconde, nous pouvons suivre le déplacement des globules rouges dans les mailles du réseau et quantifier le débit sanguin à n’importe quel point du réseau, en y mesurant la concentration et la vitesse des globules rouges », explique la chercheuse. « Ces expériences nous permettent d’étudier le lien entre l’organisation des capillaires et leur fonction, à savoir transporter le sang et donc l’oxygène et les nutriments jusqu’aux cellules du cerveau. Mais nous analysons également les conséquences d’un changement de cette organisation, lorsqu’un des canaux s’obstrue par exemple ».

En intégrant les données issues de ces situations simplifiées mais fidèles à la réalité des écoulements sanguins, les chercheurs peuvent les extrapoler à des situations plus complexes. Ils ont ainsi déjà élaboré des modèles numériques de l’écoulement du sang dans un vaisseau mais aussi dans des réseaux composés de 15 000 à 1 000 000 de vaisseaux ! L'originalité de ces modèles réside dans la prise en compte, à chaque échelle, des phénomènes physiologiques complexes prépondérants, comme la présence des globules rouges par exemple dans les modèles d’écoulement du sang.
Une base de données anatomiques unique au monde
Pour s’approcher plus près de la réalité de la microcirculation sanguine chez l’humain, les chercheurs s’appuient sur deux ressources très spécifiques : des données anatomiques humaines et des expériences d’imagerie chez l’animal.
Le projet BrainMicroFlow bénéficie en effet d’une base de données anatomiques unique au monde. Initiée par l’équipe Inserm du Centre de neuro-imagerie de Toulouse, elle renferme des coupes anatomiques du système capillaire de cerveaux humains, issues de prélèvements post-mortem sur des personnes saines. Autant de photographies qui livrent de précieuses informations sur l’architecture normale des capillaires. À terme, cette bibliothèque devrait être enrichie de tissus prélevés cette fois-ci sur des personnes atteintes de la maladie d’Alzheimer, ce qui permettrait de comparer les architectures.
Par ailleurs, pour disposer de données sur la fonction des capillaires, les chercheurs recourent à l’imagerie in vivo chez la souris. La technique, développée par les partenaires américains du projet permet d’observer en direct le déplacement des globules rouges dans le cerveau. Pionniers dans cette technique d’imagerie laser, ils sont aussi capables de boucher sélectivement un seul vaisseau préalablement choisi et de mesurer en temps réel l’impact de cette occlusion sur l’écoulement sanguin. « Ce sont des données précieuses pour valider nos modèles, d’autant qu’elles correspondent précisément aux perturbations que nous mettons en cause dans notre approche de la maladie d’Alzheimer. »
nous pourrons comprendre l'écoulement sanguin et les échanges moléculaires.
À mi-parcours du projet, les chercheurs visent plus loin. Leur prochain objectif est de mettre au point, grâce aux modèles de simulation de la microcirculation sanguine cérébrale, des modèles décrivant les échanges moléculaires (oxygène, nutriments, déchets métaboliques) qui ont lieu entre le sang et les cellules du cerveau. L’enjeu serait de déterminer comment les altérations de l’architecture des capillaires (réduction de leur nombre, obstructions, etc.) induisent des baisses de performances fonctionnelles du système microvasculaire, elles-mêmes susceptibles d’entraîner la dégénérescence des neurones.
« Ainsi, grâce à l’ensemble de nos simulations numériques, nous pourrons comprendre et mettre en images l’écoulement sanguin à différentes échelles du cerveau ainsi que les échanges moléculaires, explique Sylvie Lorthois.
Une fois ces modèles validés à partir des mesures in vivo réalisées chez la souris, nous les transposerons à l’humain grâce à nos données anatomiques, en prenant en compte les différences d’architecture cérébrales entre les deux espèces. »
Ces travaux devraient ouvrir la voie à de nouvelles stratégies de diagnostic et de suivi du fonctionnement cérébral, que ce soit dans le cas du vieillissement normal, de la maladie d’Alzheimer ou même d’autres pathologies neurologiques. Si les chercheurs parviennent à relier les changements dans l’organisation physique des vaisseaux capillaires à des modifications biologiques, comme une baisse du débit sanguin, il deviendra possible en détectant ces signaux biologiques de déduire l’existence d’altérations dans le maillage des capillaires et, in fine, d’y remédier. De nouvelles stratégies de traitement pourraient alors voir le jour...
Voir aussi
Auteur
Rédactrice scientifique depuis plus de dix ans, Stéphanie Belaud s’est notamment spécialisée dans les domaines de la biologie, de la médecine et de l’environnement.