A la une

La biocatalyse est en plein essor, captivant notamment l’attention de l’industrie pharmaceutique en quête de procédés de synthèse innovants pour fabriquer des principes actifs de médicaments. Xavier Guinchard, directeur de recherche CNRS à l'Institut de chimie des substances naturelles[1], vient de mettre au point une stratégie prometteuse, simple, efficace, et éco-compatible pour la synthèse d’amines chirales, reposant sur la combinaison d’une catalyse par l’or combinée à celle d’une enzyme.
Xavier Guinchard, chimiste organicien, s'intéresse depuis une quinzaine d’années aux processus catalytiques permis par les complexes d’or, son métal de prédilection. Il est spécialisé dans la catalyse énantiosélective, qui permet de contrôler le phénomène de chiralité des molécules du Vivant. « La caractéristique de deux molécules énantiomères est de ne pas être superposables l’une à l’autre, comme la main droite ne l’est pas à la main gauche, explique le chercheur. Elles peuvent être soit d'une forme, soit de l'autre. L’idée est donc de contrôler la stéréochimie des molécules en favorisant la formation de l'une des formes par rapport à l'autre ».
Coordonné par Xavier Guinchard, le projet ANR BiAuCat réunissait une équipe de l’ICSN incluant une doctorante et un post-doctorant, ainsi que l’équipe ChemSyBio dirigée par Olivier Berteau, chercheur de l'INRAE spécialiste en biocatalyse. Ce projet a été financé par l’Agence nationale de la recherche (ANR), dont l’objectif est de soutenir l’excellence de la recherche et l’innovation française sur le plan national, européen et international. Son principal objectif était de créer des processus catalytiques innovants et éco-compatibles combinant la catalyse enzymatique avec la catalyse à l’or, deux systèmes catalytiques radicalement différents dans un même récipient, accélérant ainsi la production de molécules complexes, tout en contrôlant leur stéréochimie.
Transformer les alcynes en amines chirales
L’une des avancées majeures du projet est d’avoir réussi à convertir des alcynes (des hydrocarbures caractérisés par leur triple liaison carbone-carbone) en amines chirales. « On part de quelque chose issu du pétrole, très peu fonctionnalisé et avec principalement du carbone et de l'hydrogène et peu cher, pour arriver à une amine chirale, qui présente au contraire un haut niveau de fonctionnalisation et dont le motif est très proche de celui de nombreux médicaments », détaille Xavier Guinchard.
Le processus débute par une hydratation des alcynes catalysée par le complexe d'or générant une cétone dans le milieu réactionnel, suivie de la transformation catalysée par une transaminase en amine chirale, une étape presque entièrement stéréosélective. « Nous avons démontré l’incroyable efficacité de ces enzymes en termes de stéréosélectivité, c'est-à-dire du contrôle de la chiralité. Ceci contredit d’ailleurs l'idée répandue selon laquelle les enzymes sont spécifiques à un seul substrat. », affirme le chercheur. La démarche est, de plus, parfaitement éco-compatible puisque les réactions utilisent l’eau comme solvant et des catalyseurs enzymatiques renouvelables.
Une capacité à monter en échelle
Contrairement à d’autres études sur le sujet, les résultats obtenus par l'équipe de BiAuCat sont significativement supérieurs en termes d'échelle et de praticité. L'équipe a démontré la robustesse de la méthode en l'appliquant à la synthèse de plusieurs médicaments, dont le clobenzorex, un coupe-faim, et la lisdexamfétamine, utilisée pour traiter les troubles de l'attention.
« Nous avons réussi à opérer à une échelle de 6 mmol, produisant près d’un gramme de produit final en une seule fois, se félicite le chimiste. Cette capacité à monter en échelle représente parfois un véritable défi en biocatalyse ». Autre avantage, la simplicité remarquable du processus : « La méthode ne nécessite pas de précautions particulières. Le mélange réactionnel avec nos deux catalyseurs est constitué principalement d'eau comme solvant ; le tout est agité à l’air dans le laboratoire à une température de 30 °C. Ces conditions simples pourraient rendre notre stratégie d’autant plus exploitable pour l’industrie pharmaceutique », conclut le chercheur.
Perfectionner la multi-catalyse
Convaincu de l'intérêt de la stratégie développée, Xavier Guinchard poursuit ses recherches, explorant des réactions encore plus élaborées, où les deux activités catalytiques, par l'enzyme et le complexe d'Au(I), seraient encore plus perfectionnées, tout en utilisant des procédés respectueux de l'environnement. Ces découvertes permettent d'envisager des utilisations inédites en synthèse organique, ouvrant notamment des perspectives novatrices pour la création rapide de molécules bioactives chirales.
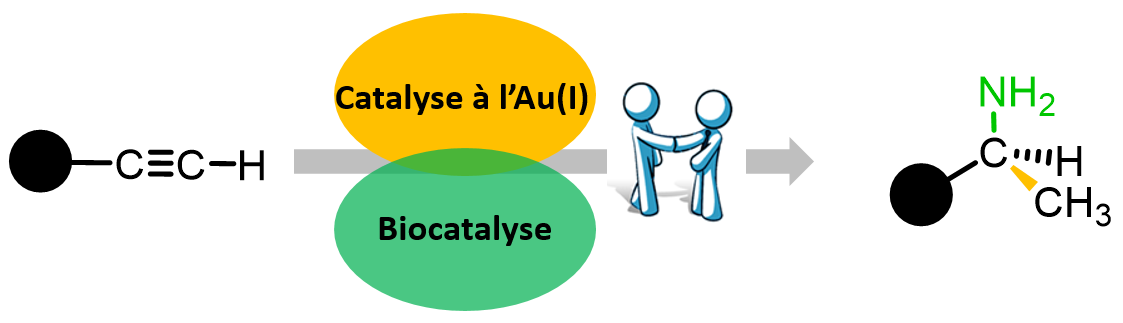
Légende :
Le projet BiAuCat : combiner la catalyse à l’or et la biocatalyse pour la synthèse de briques.
© Xavier Guinchard/ICSN



