A la une

Bien qu’on les croise accrochées à des rochers ou souvent échouées sur les plages, les algues renferment des trésors. Elles sont en effet principalement constituées de longues chaînes de sucres, appelées polysaccharides, qui jouent un rôle proche de celui de la cellulose chez les plantes et les arbres. Les oligosaccharides sont des fragments de polysaccharides, des molécules plus petites ayant souvent des propriétés bioactives qui intéressent de nombreuses industries : cosmétique, pharmaceutique, biomédicale, etc.
Parmi ces polysaccharides, les alginates, tirés des algues brunes qui peuplent les écosystèmes côtiers des régions tempérées et polaires, sont ainsi employés comme épaississants, gélifiants, émulsifiants et stabilisants, pour encapsuler des médicaments, dans la lessive ou encore pour réaliser des empreintes dentaires. Les algues brunes comptent également parmi leurs polysaccharides des fucanes sulfatés, dont les oligosaccharides ont montré des propriétés antioxydantes, anti-infectieuses, cicatrisantes et boostant le système immunitaire. Mais, contrairement aux alginates, ces molécules d’intérêt ne sont pas extraites à grande échelle et il n’y a pas d’enzymes spécifiques, disponibles commercialement, pour produire des oligosaccharides de fucanes. Cela limite leur utilisation par l’industrie, et c’est là qu’intervient Gurvan Michel.

Tableau représentant des algues, et qui a servi de couverture à un numéro d’Environmental Microbiology © Corinne Michel
Le rôle crucial des enzymes
Ce biochimiste, directeur de recherche CNRS à la Station biologique de Roscoff1, étudie les enzymes des bactéries et des grandes algues marines en combinant cristallographie et génomique. Les enzymes étant de petites protéines fabriquées par les cellules afin de faciliter les réactions chimiques dont elles ont besoin pour vivre.
« Comme les champignons colonisent de vieilles souches d’arbres, des bactéries qui se nourrissent des oligosaccharides dégradent progressivement les algues mortes, développe Gurvan Michel. Elles ne peuvent en effet pas assimiler directement les polysaccharides, qu’elles doivent d’abord découper en fragments jusqu’à la libération de sucres simples. J’explore les fonctions et la structure tridimensionnelle des enzymes produites par des bactéries marines dont on connaît le génome complet. À partir de là, je peux identifier quelles protéines parviennent à diviser les polysaccharides à tel ou tel endroit de leur chaîne. »
La Station biologique de Roscoff dispose depuis une trentaine d’années d’une équipe qui décrypte les voies métaboliques complexes liées aux polysaccharides des algues. Gurvan Michel et ses collègues ont ainsi découvert en 2006 une première bactérie marine, baptisée Mariniflexile fucanivorans, capable de découper les fucanes sulfatés grâce à certaines de ses enzymes, les fucanases. Chacune fonctionne comme un petit ciseau qui ne s’attaque qu’à une partie spécifique de la chaîne, mais il est difficile d’identifier qui fait quoi dans ce cocktail aussi varié que minuscule.
Une enzyme dans une botte de protéines
« Une bactérie produit en moyenne cinq mille protéines, et nous devons en trouver une seule, explique Gurvan Michel. Avec les méthodes classiques de séparation des molécules, on se retrouve avec des quantités extrêmement faibles de protéines et il faudrait une somme de travail équivalente à deux doctorats complets pour isoler une enzyme sauvage, identifier son gène correspondant et étudier son mode d’action sur le polysaccharide ciblé. »
À la place, Gurvan Michel a coordonné le séquençage complet du génome de Mariniflexile fucanivorans, et ainsi repéré un groupe d’une vingtaine de gènes qui pourraient être liés à la biodégradation des fucanes sulfatés. Il lui a ensuite fallu cloner et surexprimer chacun de ces gènes pour produire et purifier les enzymes correspondantes. Cette étape est nécessaire pour pouvoir caractériser chaque enzyme et déterminer leur rôle exact dans le découpage ou la modification de ces polymères complexes.
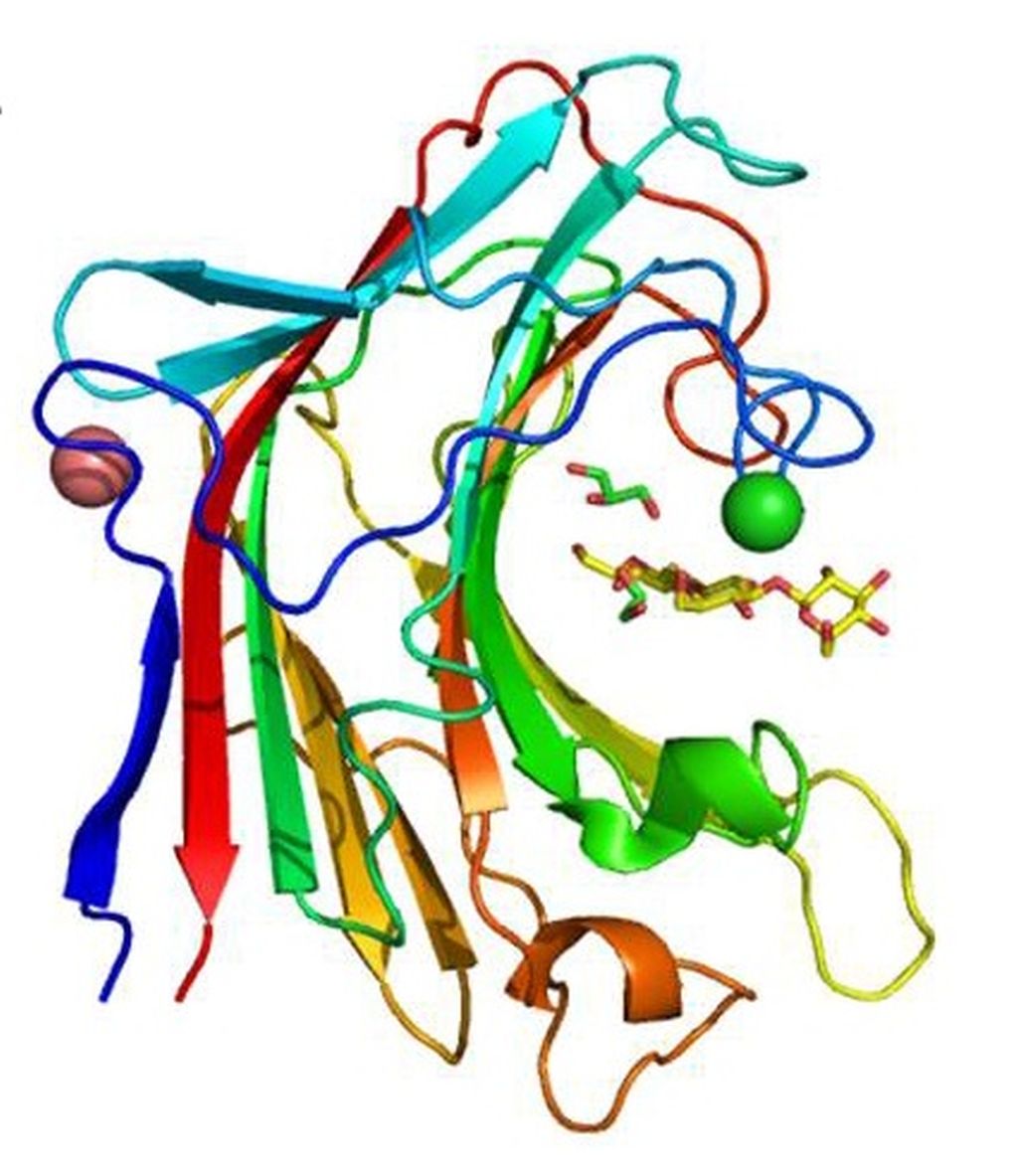
La laminarinase LamC de Zobellia galactanivorans © Gurvan Michel / Station biologique de Roscoff.
Vingt et une enzymes caractérisées
Pour cette phase de surexpression des protéines candidates, Gurvan Michel et ses collègues ont utilisé des Escherichia coli, des bactéries très prisées des chercheurs pour leur capacité à se multiplier rapidement et à produire de grandes quantités d’enzymes. Pour la caractérisation de l’activité biochimique de ces nouvelles enzymes, l’équipe a reçu l’aide de collègues de la plateforme Bioressources : imagerie, biochimie & structure (BIBS) de l’INRAE de Nantes, spécialisés dans la caractérisation des oligosaccharides par spectrométrie de masse.
Vingt et une enzymes d’intérêt ont ainsi été identifiées et décrites, les détails seront publiés dans un article scientifique encore en cours de rédaction. Certaines pourraient servir à AberActives, une startup fondée fin 2021 par Gurvan Michel et des collègues de la Station biologique de Roscoff. L’entreprise développe en effet des approches de bioraffinerie des algues, encore une fois à l’aide d’enzymes, adaptées aux besoins des industriels. Sa mission se déroule dans le même esprit d’utiliser des protéines naturelles pour des réactions chimiques plus vertes, aboutissant à des produits à haute valeur ajoutée.
-----------------------------------------------------------------------------------
Ces recherches ont été financées en tout ou partie, par l’Agence Nationale de la Recherche (ANR) au titre du projet Découverte d’enzymes pour le contrôle des propriétés biotechnologiques des fucanes sulfatés — Breaking_Alg – AAP 2018-2019. Cette communication est réalisée et financée dans le cadre de l’appel à projet Sciences Avec et Pour la Société - Culture Scientifique Technique et Industrielle pour les projets JCJC et PRC des appels à projets génériques 2018-2019 (SAPS-CSTI-JCJC et PRC AAPG 18-19).
- 1. Unité CNRS / Sorbonne Université



