A la une

Et si la clé de la longévité cellulaire déclenchait l'obésité ? C'est le paradoxe de THALATEL : en voulant protéger nos neurones du vieillissement, les chercheurs ont découvert un rôle inédit de la télomérase dans la gestion de notre faim.
Dans l'intimité de nos tissus, le temps laisse une trace indélébile : l’accumulation de cellules sénescentes. Ces cellules "zombies", qui ne se divisent plus mais restent métaboliquement actives, sont aujourd'hui identifiées comme le dénominateur commun de nombreuses pathologies liées à l’âge, de l’arthrose au diabète. Si ce mécanisme de sénescence est crucial en début de vie pour stopper la prolifération des tumeurs, son accumulation excessive finit par créer une inflammation chronique, locale puis systémique.
Au bout de chaque chromosome, le raccourcissement des télomères - ces capuchons protecteurs de notre ADN - sonne normalement l'heure de cette retraite cellulaire. Pour contrer ce déclin, l'enzyme chargée de les maintenir, la télomérase, apparaît comme une candidate idéale. C'est l'ambition du projet THALATEL, porté par Vincent Géli (Directeur de recherche CNRS à l’IRCAN à Nice) et une collaboration d’experts incluant Franck Oury, Laura Braud, Jean-François Tanti, et Vincent Prévot.
Un "coup de pouce" génétique chirurgical
L'idée à l'origine du projet est aussi audacieuse que précise : que se passe-t-il si l'on apporte un "coup de pouce" à la télomérase uniquement lorsque la cellule commence à basculer vers la sénescence ? Pour le savoir, les chercheurs ont conçu un modèle de souris génétiquement modifié, baptisé p21-TERT. Ici, le gène codant pour la sous-unité catalytique de la télomérase (TERT) est placé sous le contrôle du promoteur du gène p21, un médiateur clé qui s'active à la suite de nombreux stress.
« C'était une intuition théorique forte », explique Vincent Geli. « L'idée initiale était que si on utilisait la télomérase pour réparer les télomères dysfonctionnels, on pourrait inverser la sénescence cellulaire. Cette idée est toujours vraie, mais ce qu'on n'avait pas prévu, c'est que TERT abroge aussi la sénescence à travers beaucoup d'activités "non-canoniques" - des fonctions qui ne sont pas liées à l'allongement des extrémités des chromosomes - et c'est ce que nous mettons aujourd'hui en évidence. »
Les premiers résultats, publiés en 2024 avec l’équipe de Serge Adnot (Hôpital Mondor, Créteil (Travaux de Larissa Lipskaia1), ont eu des airs de victoire contre le temps : en activant ce mécanisme dans des poumons vieillissants de souris, l'équipe a réussi à obtenir « des souris vieilles avec des poumons jeunes et une vasculature préservée ». Cependant, la nature ne se laisse pas dompter si facilement. Les chercheurs ont observé que 15 % de ces souris développaient des tumeurs au foie, même lorsque la télomérase était catalytiquement inactive. Une surprise majeure qui confirme que TERT influence le métabolisme des cellules bien au-delà de la simple protection de l’extrémité des chromosomes.
 Injection des AAV9-shTERT permettant d'éteindre l'expression de Tert dans l'hypothalamus © Ines Martinez-Corral
Injection des AAV9-shTERT permettant d'éteindre l'expression de Tert dans l'hypothalamus © Ines Martinez-Corral
Le point de bascule : quand l'anti-âge fait grossir
C’est en explorant les liens entre stress et métabolisme que le projet a pris un tournant spectaculaire. Soumises à un régime riche en graisses (High Fat Diet), les souris p21-TERT ont d'abord montré une résistance étonnante : elles préservaient le fonctionnement des cellules souches adipocytaires et évitaient l'inflammation massive du tissu adipeux (Travaux de Laura Braud et Collaborateurs publiés en 2025 et 20262-3).
Pourtant, un mystère persistait. Vers l’âge de 10 mois, ces souris "protégées" ont commencé à manger de manière compulsive, entraînant une prise de poids marquée. Le coupable n’était pas dans le ventre, mais dans la tour de contrôle du corps : l’hypothalamus. Cette zone du cerveau abrite les neurones spécifiques qui régulent la satiété et l’appétit.
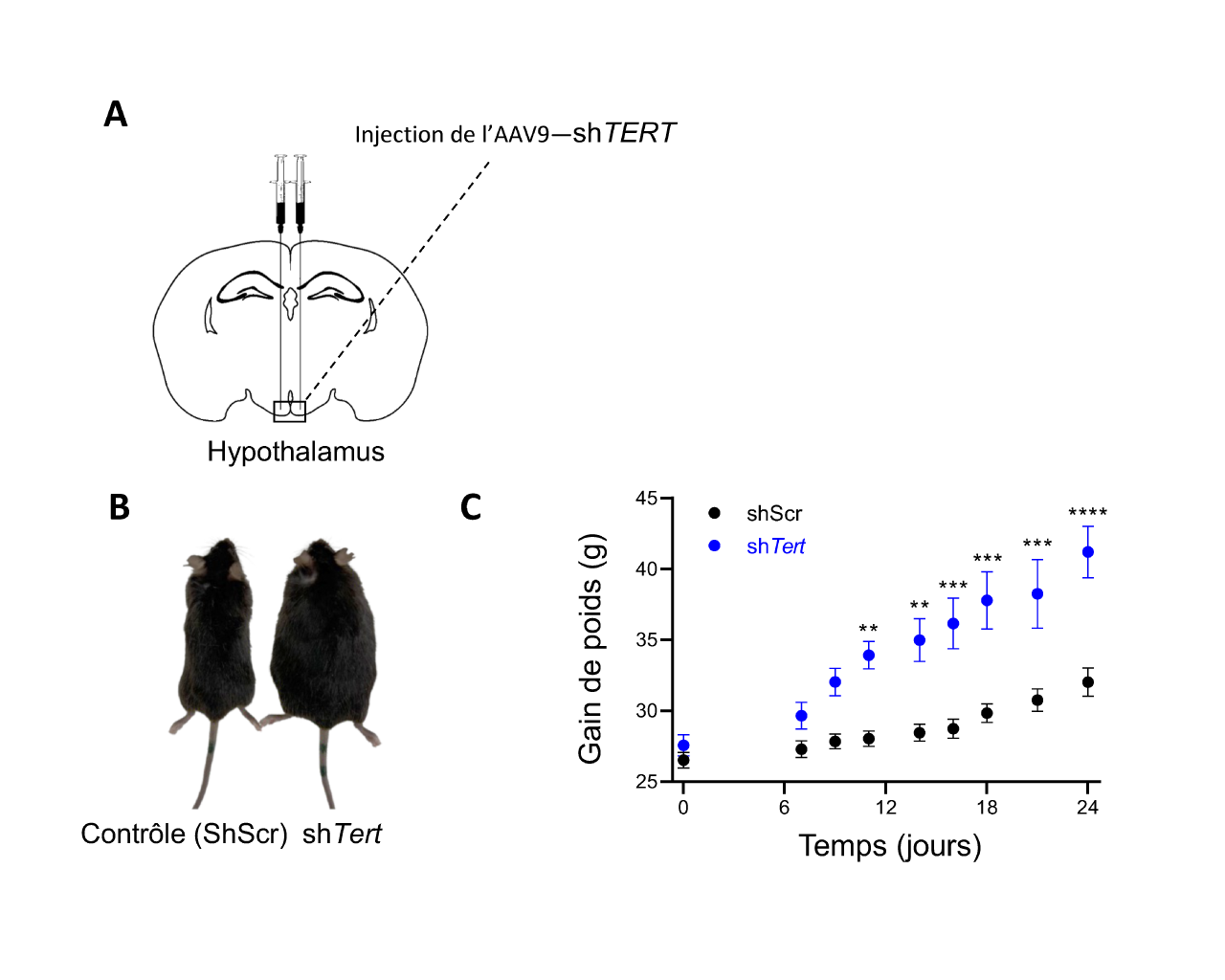 Gain de poids chez les souris après injection d’un AAV visant à réduire l’expression de TERT au sein de l’hypothalamus © Vincent Geli
Gain de poids chez les souris après injection d’un AAV visant à réduire l’expression de TERT au sein de l’hypothalamus © Vincent Geli
L'obésité, une maladie du cerveau vieillissant ?
Pour valider cette piste, Michel Leivovici et Miranda Bueno-Arribas de l'équipe de Franck Oury, en collaboration avec Ines Martinez et Ariane Sharif à Lille, ont mené une expérience radicale : éteindre l'expression de TERT spécifiquement dans l'hypothalamus de souris normales via l'injection d'un virus (AAV).
« C'était encore plus spectaculaire que nos premiers résultats ! », s'enthousiasme Vincent Géli. « En éteignant la télomérase dans l'hypothalamus, on a vu les souris grossir à une vitesse grand V, provoquant une dérégulation des mécanismes de la faim en seulement trois semaines. Nous pensons que la perte de TERT affecte directement le métabolisme des neurones, peut-être en diminuant leur protection contre le stress oxydant. »
Cette découverte renverse le paradigme habituel. Elle suggère que dans nos neurones, la télomérase n'est pas une ouvrière du bâtiment pour les télomères, mais un véritable bouclier protecteur. Sans elle, l’équilibre des neurones contrôlant la satiété est perturbé, modifiant ainsi le comportement alimentaire. En reliant cerveau et métabolisme, THALATEL dessine une nouvelle cartographie du vieillissement, où la télomérase apparaît comme un acteur important et inattendu de notre équilibre énergétique.
Perspectives : des neurones aux articulations
La dernière phase du projet, qui court jusqu'en décembre 2026, s’attache à décrypter ce mystère moléculaire, un travail qui sera poursuivi via une nouvelle ANR (HypoTERT). Au-delà de la compréhension fondamentale, des applications concrètes émergent déjà. L’équipe de Jean-Marc Brondello (IRMB, Institut de Médecine Régénératrice et Biothérapies, Montpellier) a notamment montré un rôle protecteur de TERT dans des modèles d’arthrose.
Les équipes de Montpellier travaillent désormais sur l'utilisation de "vésicules extracellulaires" pour délivrer les effets anti-inflammatoires de la télomérase sans les risques liés à la manipulation génétique. Une demande de maturation est en cours auprès de la SATT pour traiter l'obésité et l'arthrose via cette voie innovante. En conclusion, l’ANR THALATEL a mis en lumière de multiples rôles de TERT ouvrant de nouveaux horizons thérapeutiques.
1Lipskaia et al. EMBO Rep 25 (2024).
2Braud et al. Mol Metab 102262 (2025).
3Braud et al. biorxiv.org/content/10.64898/2025.12.18.694395v1 (2026).
Projet THALATEL, porté par Vincent Géli (Directeur de recherche CNRS au CRCM puis à l’IRCAN à Nice) est une collaboration d’experts incluant Franck Oury (Hôpital Necker-Enfants malades), Laura Braud (Centre de Recherche en Cancérologie de Marseille, CRCM), Jean-François Tanti (Centre Méditerranéen de Médecine Moléculaire, Nice), et Vincent Prévot (Centre de Neuroscience et Cognition, Lille).
____
Ces recherches ont été financées en tout ou partie, par l’Agence nationale de la recherche (ANR) au titre du projet ANR - THALATEL- AAPG22. Cette communication est réalisée et financée dans le cadre de l’appel à projet Sciences Avec et Pour la Société - Culture Scientifique Technique et Industrielle pour les projets JCJC et PRC des appels à projets génériques 2022 (SAPS-CSTI-JCJC et PRC AAPG 22).



