Vous êtes ici
La lumière à l’assaut du cancer
Temps de lecture : 7 minutes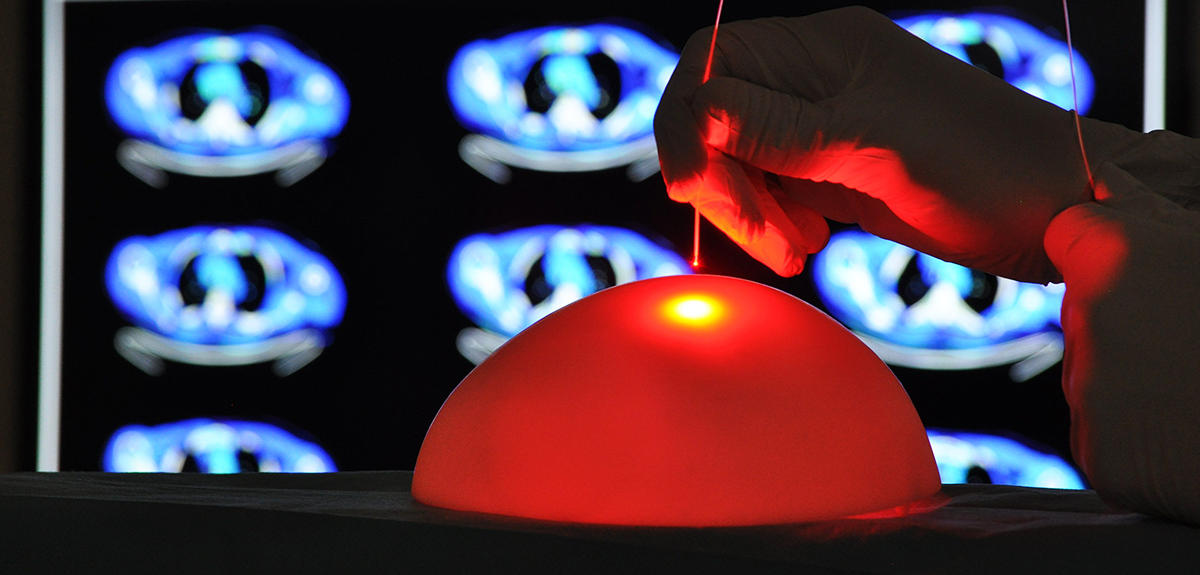
Fin octobre 2017 au CHRU de Lille, neuf patients atteints de glioblastome, une tumeur incurable du cerveau, ont bénéficié d’un traitement inédit par thérapie photodynamique (PDT). Cette technique permet de cibler sélectivement et localement les cellules cancéreuses isolées grâce à une molécule sensible à la lumière.
En France, les traitements par thérapie photodynamique ont débuté dès les années 1980. En dermatologie comme en oncologie, cette technique en pleine évolution représente un nouvel espoir de traitement pour des pathologies souvent inopérables.
Une réaction photochimique
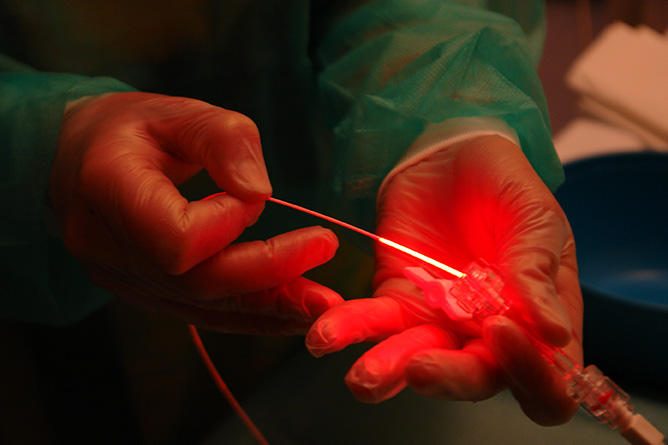
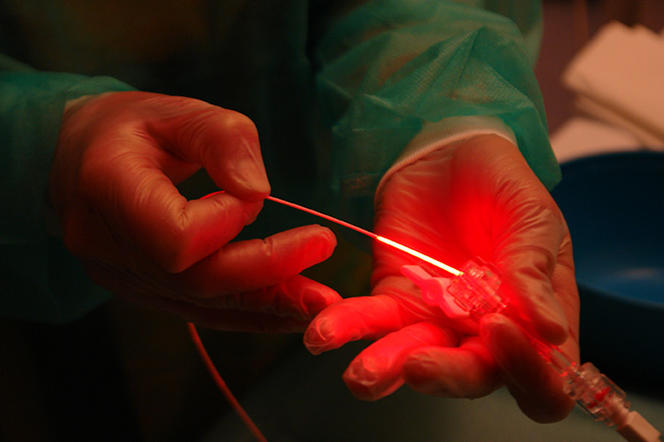
Comment agit la PDT ? « Trois éléments entrent en jeu, explique Céline Frochot, directrice de recherche au Laboratoire réactions et génie des procédés1, et coorganisatrice de cette journée : la lumière, des photosensibilisateurs – des médicaments sous forme de pommade ou injectés par intraveineuse – et l’oxygène, présent naturellement dans l’organisme. C’est la concomitance de ces trois éléments qui va créer une réaction photochimique. La lumière est émise à l’aide d’une lampe LED, d’un laser, de textiles lumineux ou par fibres optiques lorsque les lésions à traiter sont internes. Elle réagit avec les molécules photoactivables, les excite et excite l’oxygène qui devient toxique à la lumière. Ce stress oxydant va détruire les cellules malades. »
En effet, les cellules cancéreuses possèdent des récepteurs en surnombre sur leur membrane et sont incapables d’éliminer l’agent photosensibilisateur qui va venir se fixer sur elles. « Si l’on applique ces molécules photosensibilisantes en excès, les cellules cancéreuses les retiennent en excès : le différentiel entre cellules normales et tumorales est très important. Grâce à la PDT, on ne détruit que les cellules malades et on préserve les cellules saines », poursuit le biophysicien Serge Mordon, directeur de l’unité Inserm « Thérapies interventionnelles assistées par l’image et la stimulation » et coorganisateur du colloque.
Un traitement de référence pour les lésions cutanées précancéreuses
C’est en dermatologie que la thérapie photodynamique est le plus fréquemment utilisée, pour traiter les dommages causés par le soleil comme les kératoses actiniques.
« C’est le premier motif de consultation en dermatologie : Ces lésions de la peau touchent près de 3,5 millions de personnes en France, plus particulièrement les hommes âgés et chauves. Les kératoses actiniques sont des lésions précancéreuses, mais qui peuvent évoluer en carcinome épidermoïde. Il est donc nécessaire de les traiter », explique Serge Mordon. « L’intérêt de la PDT, c’est que l’on peut traiter les lésions visibles et celles, microscopiques, que l’on ne voit pas encore », poursuit-il. Bien moins douloureuse que la chirurgie, la PDT ne laisse aucune cicatrice.
Le chercheur et son équipe ont par ailleurs développé un nouveau dispositif appelé Phos-Istos, un textile lumineux souple qui, après application d’une crème sur la zone à traiter, permet une illumination moins forte mais sur une durée plus longue, afin de diminuer les effets secondaires de l’exposition à la lumière. Actuellement, seuls deux agents photosensibilisants sont disponibles en France pour la PDT. « Mais nous travaillons actuellement à l’élaboration de nouveaux composés qui interagissent encore plus efficacement avec la lumière pour mieux cibler les cellules malades, explique Céline Frochot. Il s’agit là de lier les deux versants, de la recherche fondamentale au protocole clinique. La recherche pluridisciplinaire est indispensable pour améliorer cette nouvelle approche thérapeutique. »

Une alternative thérapeutique pour le cancer de la prostate
La PDT est actuellement à l’étude pour des cancers dont l’évolution est lente et la survie bonne, comme le cancer de la prostate. « C’est le premier cancer chez l’homme de plus de 50 ans dans les pays industrialisés. Auparavant, lorsque l’on détectait un cancer de la prostate, on opérait chirurgicalement. Mais la prostatectomie entraîne dans 30 % à 40 % des cas des troubles urinaires et sexuels. Il y a un risque de suropération. »
Lors d’un essai clinique réalisé entre 2014 et 2015, l’évaluation de la PDT a été menée à l’aide d’un nouveau photosensibilisateur développé par une société française : sur une cohorte de 413 patients diagnostiqués au stade précoce, 207 étaient sous surveillance active ; une IRM était réalisée tous les 4 à 6 mois afin de suivre l’évolution des lésions. Les 206 autres patients ont été traités par PDT. Après un an de suivi, 14 % des patients en surveillance active avaient une biopsie négative contre 49 % des patients traités par la thérapie photodynamique. « Avec 70 000 nouveaux cas de cancer de la prostate par an, il est difficile d’avoir un suivi par IRM régulier. La PDT représente donc une véritable alternative thérapeutique. » La PDT permet également de traiter des tumeurs très invasives pour lesquelles la médiane de survieFermerdélai dans lequel la moitié des malades est décédée est de quelques mois, comme le mésothéliome – le cancer lié à l’amiante –, ou le glioblastome.
Une première mondiale pour le glioblastome
Cette tumeur très agressive du cerveau vient de faire l’objet d’une première mondiale au CHRU de Lille, où cinq patients atteints de glioblastome participent depuis mai 2017 à un essai clinique incluant la thérapie photodynamique.
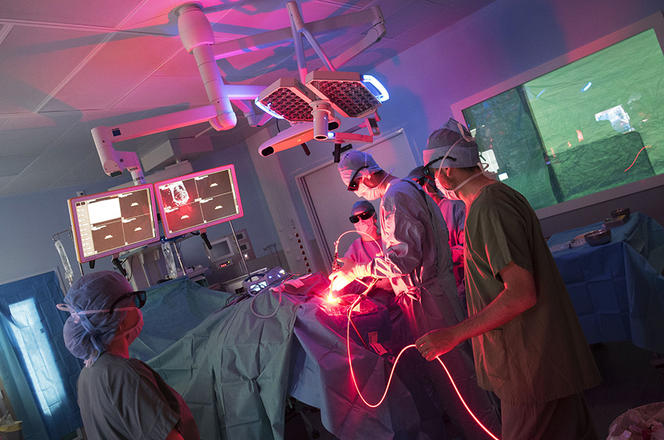
Pour les malades, le pronostic est sombre : la médiane de survie est inférieure à 15 mois. Le glioblastome est une tumeur infiltrante qui double de volume tous les mois. Et malgré l’ablation de la tumeur, les récidives sont fréquentes. En cause, certaines cellules malades qui ne peuvent pas être retirées chirurgicalement. Pour Serge Mordon, il s’agit d’intégrer cette thérapie au parcours de soins standard, en complément de l’arsenal thérapeutique classique – chirurgie, chimiothérapie et radiothérapie.
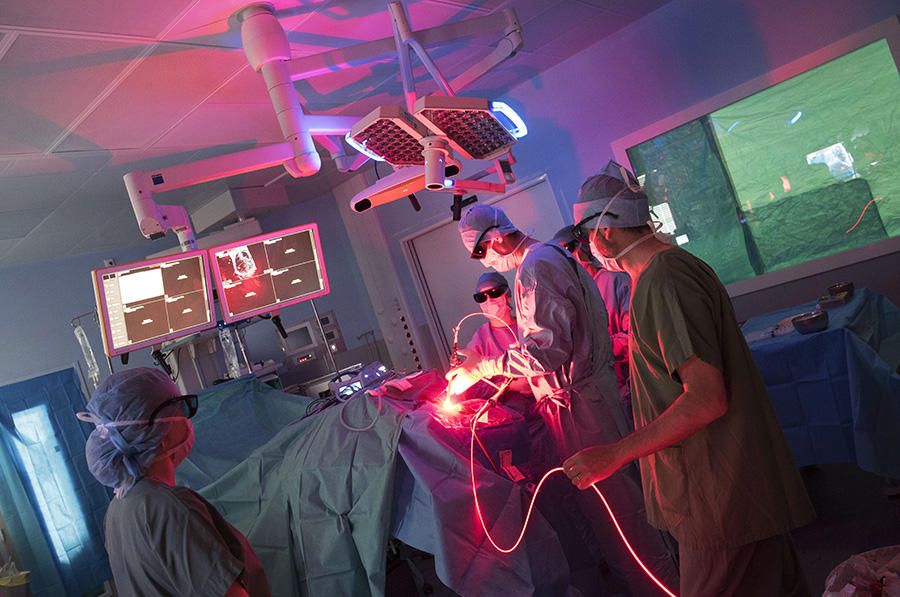
« Quelques heures avant l’opération, le patient reçoit l’injection d’une molécule photosensibilisatrice qui se diffuse dans tout le corps et va se fixer sur les cellules cancéreuses. Grâce à une lumière bleue, la tumeur est plus facilement repérable par le neurochirurgien qui va pouvoir retirer le maximum de la tumeur sans causer de lésion neurologique. Une IRM permet ensuite de visualiser ce qui reste de la tumeur. Nous intervenons ensuite, pour illuminer avec la bonne lumière, la bonne dose et au bon endroit ». Cinq illuminations pendant une quinzaine de minutes où un ballonnet est placé dans la cavité crânienne et éclaire de manière homogène le champ opératoire par une lumière rouge – une longueur d’ondes qui pénètre plus profondément dans les tissus. Dans quelques mois2, cliniciens et chercheurs pourront ainsi évaluer l’efficacité de la thérapie photodynamique dans le traitement du glioblastome.
En savoir plus :
Journée française sur la thérapie photodynamique, à l’institut de biologie de Lille, le 30 novembre 2017.
Voir aussi
Auteur
Formée au journalisme scientifique, Anne-Sophie Boutaud collabore régulièrement avec CNRS Le Journal. Elle s’intéresse à tous les sujets, de l’infiniment grand à l’infiniment petit, avec une appétence particulière pour les domaines de l’environnement, des sciences humaines et sociales, et de la santé