A la une
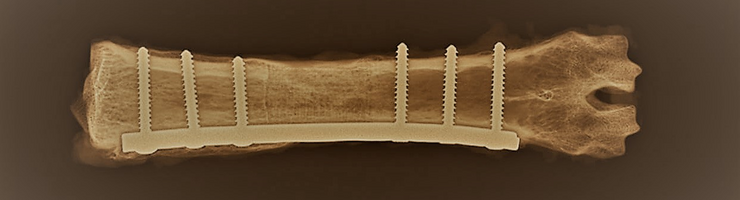
Un laboratoire grenoblois est parvenu à guérir un os sévèrement fracturé à l’aide d’un implant en 3D, enrichi d’un film bioactif qui favorise la reconstitution osseuse. Une technologie régénérative, personnalisée et sans effet secondaire, qui pourrait bien supplanter l’autogreffe et la pose d’implants synthétiques aujourd’hui pratiqués.
En principe, après une mauvaise chute, nos os disposent des propriétés nécessaires pour cicatriser de façon autonome. Toutefois, lorsque le traumatisme est violent et cause un important défaut osseux, le processus naturel de guérison peut s’avérer insuffisant. Face à cette situation, les patients se voient classiquement proposer deux options thérapeutiques : l’autogreffe osseuse et l’implant synthétique. Mais les douleurs associées à la première et l’instabilité sur le long terme de la seconde, appellent au développement d’une alternative à la fois durable et moins invasive.
Une équipe1 du laboratoire Biologie et Biotechnologies pour la Santé (Laboratoire BioSanté) et leurs partenaires2 sont en passe de relever ce défi, avec un nouvel implant poreux, biocompatible et imprimé en 3 dimensions. Il est recouvert d’un film propice à la régénération osseuse et n’induit aucun effet secondaire. Les premiers résultats obtenus témoignent d’une efficacité remarquable.
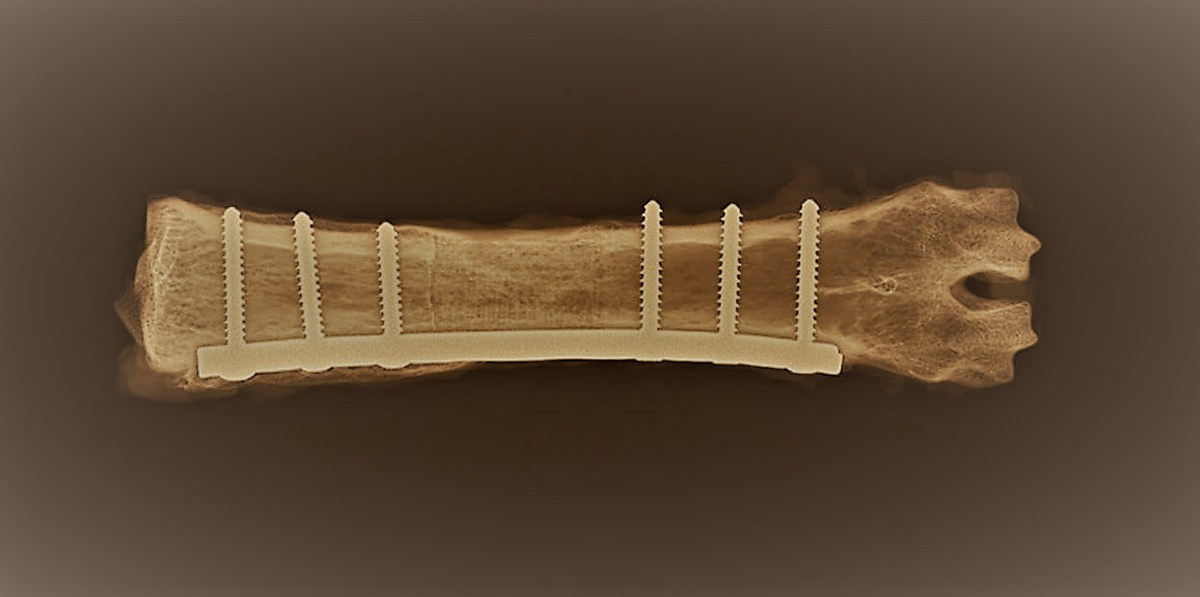
Radiographie d’un os cicatrisé à l’aide d’un implant bioactif © B3OA, École nationale vétérinaire d’Alfort
Un film bioactif ostéo-inducteur
L’équipe Biomimétisme et Médecine Régénératrice (BRM) du Laboratoire BioSanté travaille depuis 2011 sur cette technologie, dont la réussite repose sur deux propriétés distinctes : l’ostéo-induction, qui stimule la génération de nouveaux tissus osseux ; et l’ostéo-conduction, qui guide et soutient physiquement cette croissance de l’os.
Les scientifiques sont d’abord parvenus à concevoir des films bioactifs très fins « constitués de plusieurs couches de poly-lysine et d’acide hyaluronique qui sont des constituants de la matrice extra cellulaire », explique Paul Machillot, ingénieur d’étude CNRS dans l’équipe BRM. « Ces films ont la particularité d’incorporer des facteurs de croissance », poursuit-il, qui répondent au nom de code BMP2 (Human Bone Morphogenetic Protein-2). Il s’agit d’une protéine ostéo-inductrice qui permet de recruter des cellules progénitrices directement sur le site du défaut et de les spécialiser en cellules osseuses, favorisant ainsi la formation de tissu osseux.
Un implant poreux ostéo-conducteur
Les films sont assemblés directement sur la surface des mailles des implants poreux, conçus pour combler la zone osseuse endommagée. Ces structures « servent d’échafaudage aux cellules, qui peuvent s’autoorganiser, créer de l’os et combler des défauts de taille critique », développe Paul Machillot. Elles sont imprimées en 3D, façonnées « sur mesure » à partir de simples scanners et présentent l’avantage « d’épouser parfaitement le défaut osseux », pour assurer la meilleure ostéo-conduction possible.
Ces implants poreux sont, par ailleurs, « constitués de polymère synthétique biodégradable », détaille Charlotte Garot, qui a effectué et soutenu sa thèse de doctorat dans l’équipe BRM. Ce polymère est fabriqué à partir d’un composant naturel très répandu. Il est surtout biorésorbable, c’est-à-dire éliminable par les voies naturelles. « À la fin du processus de réparation, détaille-t-elle, il ne doit rester que de l’os et nous pouvons éviter que des inflammations chroniques se produisent du fait des restes d’implants ».
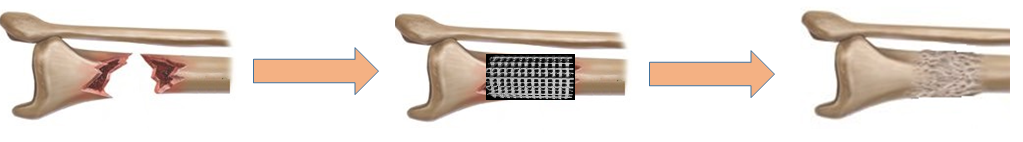
Schéma des processus d’ostéo-induction et d’ostéo-conduction permis par la pose de l’implant et l‘action du film bioactif qu’il contient © Laboratoire BioSanté
Une innovation résultant de 13 années de recherche
Le projet a nécessité de nombreuses années de recherche et de développement, depuis les premières études in vivo en 2011 jusqu’aux récents essais précliniques concluants. « Nos premières expériences visaient à démontrer l’efficacité et la compatibilité du film bioactif dans l’organisme », se souvient Charlotte Garot. Les scientifiques travaillaient alors sur différents supports : granules de céramiques, titane poreux. Ils ont pu démontrer que la protéine BMP2 était toujours active, quel que soit le support et même après stérilisation.
En 2016, le projet a pris un tournant majeur avec les premiers essais d’implants sur des os abimés de modèles vivants, en l’occurrence un fémur de rat. « Nous avons démontré à ce moment-là qu’un os initialement irréparable naturellement, pouvait se régénérer grâce à notre technologie ». Depuis, l’équipe mène des essais sur des modèles animaux de plus grande taille avec des défauts osseux plus importants (jusqu’à 12 cm3), comblés avec des implants architecturés en impression 3D.
Tout au long du processus de recherche, l’équipe BRM a mené des essais in vitro et in vivo pour tester différentes géométries d'échafaudages. Les résultats les plus récents, consécutifs à des travaux menés sur un défaut osseux du métatarse d’une brebis, ont été publiés en 2023 dans la revue Advanced Healthcare Materials. Ils montrent qu’une géométrie interne de l’implant sous forme de pores cubiques, combinée à une dose modérée de BMP2, conduisent à une régénération osseuse très efficace, sans effet indésirable et comparable aux résultats obtenus par l’autogreffe.
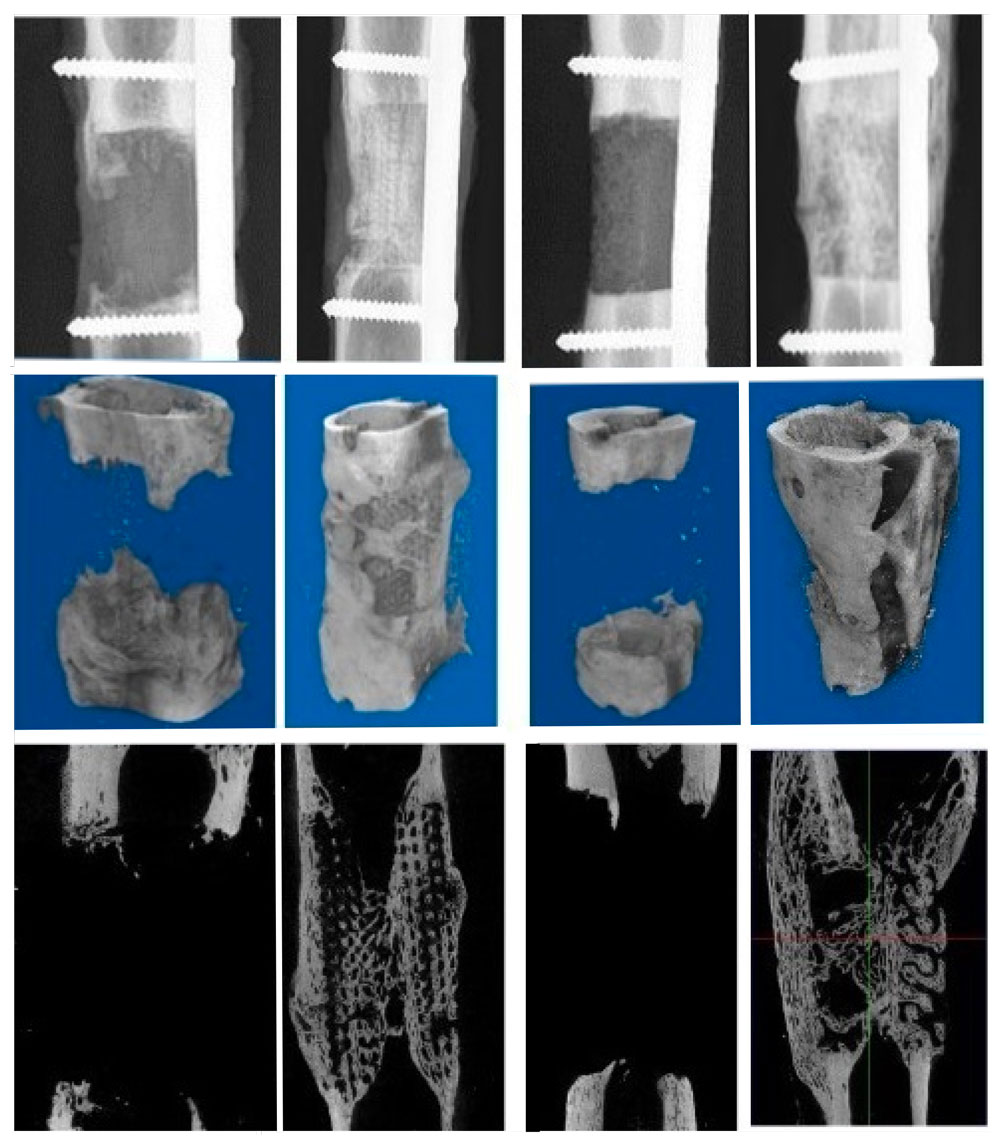
Images radiologiques (rangée du haut), images scanner 3D (rangée du milieu) et images scanner 2D (rangée du bas) montrant la reconstruction d'un métatarse de brebis avec deux échafaudages de géométries différentes et recouverts (colonnes 2 et 4) ou non (colonnes 1 et 3) de la molécule ostéo-inductrice BMP-2. © Garot et al. Adv Healthcare Materials 2023
Une solution moins douloureuse et plus durable
Il reste à optimiser cette configuration d’implants avant d’envisager une application clinique, mais les perspectives qu’ouvre cette innovation pour la régénération osseuse personnalisée sont très encourageantes. Charlotte Garot et Paul Machillot tiennent en effet à souligner que les procédés actuels présentent des limites qu’il convient de dépasser. Dans le cas d’une autogreffe osseuse « la quantité d’os prélevable n’est pas infinie et le processus reste très douloureux (…) surtout au-dessus de 10 cm3 », l’équivalent d’une balle de tennis de table. Plus le défaut est important, plus la douleur associée au prélèvement et à la greffe augmente. Par ailleurs, lorsqu’il s’agit d’un implant synthétique en céramique ou en titane, « la réparation est, certes, rapide et assez efficace, mais l’implant est inerte et empêche la reconstitution osseuse naturelle ». À long terme cela pose des problèmes de stabilité de l’implant et nécessite parfois de refaire des actes chirurgicaux.
En bonne voie vers la clinique
Avec les implants poreux bioactifs, une nouvelle stratégie de reconstruction osseuse moins douloureuse et plus durable pourrait voir le jour. Le laboratoire prépare actuellement toutes les étapes préalables au lancement d’une étude clinique avec le centre hospitalier d’Annecy Genevois, sur une dizaine de patients atteints de défauts mandibulaires majeurs. Ils pourraient bénéficier de ces implants poreux bioactifs sur mesure, pour régénérer l’os de la mâchoire et rendre possible, à terme, la pose d’un implant dentaire.
Cette prouesse biomédicale laisse entrevoir un avenir où les douleurs et les complications associées à la chirurgie osseuse appartiennent au passé, offrant aux patients une solution moins invasive et plus durable pour une guérison optimale.
_ _ _
Ces recherches ont été financées en tout ou partie, par l’Agence nationale de la recherche (ANR) au titre du projet ANR-OBOE-AAPG2018. Cette communication est réalisée et financée dans le cadre de l’appel à projet Sciences Avec et Pour la Société - Culture Scientifique Technique et Industrielle pour les projets JCJC et PRC des appels à projets génériques 2018-2019 (SAPS-CSTI-JCJC et PRC AAPG 18/19).
_ _ _
1 EMR 5000 - Biomimetism and Regenerative Medicine - BRM
2 Dans le cadre du projet ANR OBOE, en partenariat avec le CIC-IT de Bordeaux ; L’unité Ontogenèse et Oncogenèse Moléculaire de l’Institut des Biosciences Avancées (IAB) ; le Laboratoire de Biologie, Bioingénierie et Bioimagerie Ostéoarticulaires (B3OA); et le centre hospitalier Annecy-Genevois



