Vous êtes ici
Le CO2, une ressource à exploiter ?

En 2014, l’homme a émis la bagatelle de 36 milliards de tonnes de CO2 dans l’atmosphère. Une quantité encore jamais atteinte et qu’il s’agit de réduire drastiquement si l’on veut limiter la hausse de la température terrestre à 1,5 °C d’ici à la fin du siècle, comme s’y sont engagés les pays présents à la COP21. Si la principale solution reste et restera la réduction à la source des émissions de gaz à effet de serre, d’autres pistes sont aujourd’hui à l’étude pour « nettoyer » l’atmosphère de son excès de CO2. L’enfouissement en est une… Mais la solution la plus sérieusement étudiée par les chercheurs est bien plus audacieuse, puisqu’il s’agit rien moins que de considérer le CO2 de l’atmosphère comme une ressource nouvelle. En clair : l’utiliser comme une matière première !
« Dans les faits, l’industrie utilise déjà du CO2 (celui-ci est extrait du sous-sol, où on le trouve sous la forme de gisements, ou est le sous-produit de processus industriels, NDLR) pour fabriquer de l’urée, un engrais très utilisé qui peut également servir de précurseur pour de nombreux plastiques, de l’acide salicylique qui entre dans la composition de l’aspirine et de certains produits anti-acné, ou encore des polycarbonates, ces polymères qu’on retrouve dans les CD, DVD ou les verres de lunettes, raconte Marc Robert, chercheur au Laboratoire d’électrochimie moléculaire1. Soit une consommation d’environ 150 millions de tonnes de CO2 chaque année. Il s’agit d’aller plus loin dans ces usages et d’en inventer de nouveaux. »
Et bien sûr, d’utiliser pour cela le CO2 « atmosphérique ». Soit en développant des systèmes de capture du CO2 dans l’air ambiant, comme s'y emploie notamment Klaus Lakner, un chercheur de l'université d'Arizona, avec son "arbre" à CO2 - un appareil d'usage individuel qui ne pourra pas être déployé à grande échelle avant deux ou trois décennies... Soit, de façon plus réaliste, en le capturant à la sortie des cheminées d’usine où il est le plus concentré. « Des procédés très efficaces de capture en sortie d’usine existent déjà, indique François Guyot, chercheur à l’Institut de minéralogie, de physique des matériaux et de cosmochimie2. Leur principe ? Dissoudre le CO2 au pH acide dans des bains basiques placés juste au niveau de ces cheminées. »
Produire des carburants avec le CO2
Une fois capturé, les possibilités de transformation ne manquent pas : les atomes de carbone présents dans le CO2 se retrouvent en effet dans de nombreuses molécules carbonées très prisées des industriels. « À partir du CO2, on est capable de produire du monoxyde de carbone (CO), un produit de base que l’industrie chimique utilise pour fabriquer des molécules plus complexes », explique Marc Robert. Enrichi en hydrogène, le CO permet par exemple d’obtenir de l’acide formique (H-COOH), un composé liquide à température et pression ambiantes qui permettrait de faire fonctionner les piles à combustible des voitures du futur avec des risques moindres que l’hydrogène pur (H2), hautement inflammable… Plus complexe à synthétiser que l’acide formique, le méthanol (CH3OH) constitue un autre débouché d’avenir pour le CO2 : cet alcool utilisé comme solvant dans les peintures, vernis, encres…, sert aussi de carburant, pour les fusées notamment.
dix ou vingt ans
avant que ces
process soient
mûrs et
transférables
à l’industrie.
La démarche est séduisante… Mais utiliser le CO2 pour synthétiser d’autres produits carbonés à grande échelle demande de surmonter un certain nombre de difficultés. « La molécule de CO2 est très inerte, explique Marc Robert. Ses liaisons carbone-oxygène sont extrêmement solides et demandent énormément d’énergie pour les casser… D’où des dépenses importantes au niveau industriel. » Surtout, ces opérations de catalyse – car il s’agit bien de catalyse – reposent sur l’utilisation de métaux précieux tels que platine, or, argent, rhodium, iridium ou encore ruthénium, ce qui constitue un vrai frein à leur déploiement. Des centaines de laboratoires sur la planète s’emploient donc à améliorer ces processus de catalyse : en les rendant moins énergivores, et en testant des métaux non-précieux.

Marc Robert et son équipe travaillent ainsi d’arrache-pied à un procédé de catalyse utilisant le fer, le métal le plus abondant dans la croûte terrestre. « À l’heure où je vous parle, on arrive à fabriquer de façon maîtrisée du CO à partir de CO2 en utilisant des électrodes contenant du fer, s’enthousiasme le chercheur. Et ce en limitant au minimum les sous-produits issus de la catalyse, puisque nous obtenons uniquement du monoxyde de carbone, gazeux, et de l’eau liquide. » Beauté de l’expérience : toute l’électricité nécessaire à la catalyse est fournie par de petits panneaux solaires, soit une énergie 100 % renouvelable. D’autres laboratoires, notamment australiens, ont réussi à produire un mélange de CO et d’acide formique avec des électrodes au nickel ; des expériences menées avec des cristaux de cuivre réussissent, elles, à produire directement du méthanol, mais en petites quantités et mélangé à de nombreux autres sous-produits… « Il faudra encore dix ou vingt ans avant que ces process soient mûrs et transférables à l’industrie », estime Marc Robert.
Le fin du fin, pour les chercheurs, serait de produire des hydrocarbures en tout point comparables à ceux que nous utilisons aujourd’hui dans nos camions et voitures, comme l’octane (C8H18). « Certes, leur combustion libérerait à nouveau du CO2 dans l’atmosphère, mais qui serait recapturé et retransformé en carburant, et ainsi de suite… », explique Marc Robert. En clair, cela reviendrait à créer un nouveau cycle – plus vertueux – du carbone.
La nature comme source d'inspiration
Si les besoins de l’industrie chimique sont une source d’inspiration pour les scientifiques, elle n’est pas la seule. Pourquoi ne pas carrément copier les processus naturels et fabriquer… de la roche à partir du CO2 ? « La nature ne nous a pas attendus pour utiliser le CO2 de l’atmosphère, explique François Guyot. Elle s’en sert de deux manières distinctes : pour fabriquer de la biomasse, via la photosynthèse – dans ce cas, les plantes utilisent le CO2 de l’atmosphère et l’eau pour produire des sucres et de l’oxygène –, et pour fabriquer de la roche sous forme de carbonates. Exemple de ce processus dit de carbonatation, réalisé sur des périodes de plusieurs milliers d’années au cœur des océans : les falaises de craie d’Étretat ou de Douvres, entièrement constituées de carbonates de calcium (CaCO3) ! « L’intérêt de transformer le CO2 en roche est qu’il est extrêmement stable sous sa forme solide, explique le géologue. Aucun risque de le retrouver dans l’atmosphère. »
transformer
le CO2 en roche
est qu’il est
extrêmement
stable sous
sa forme solide.
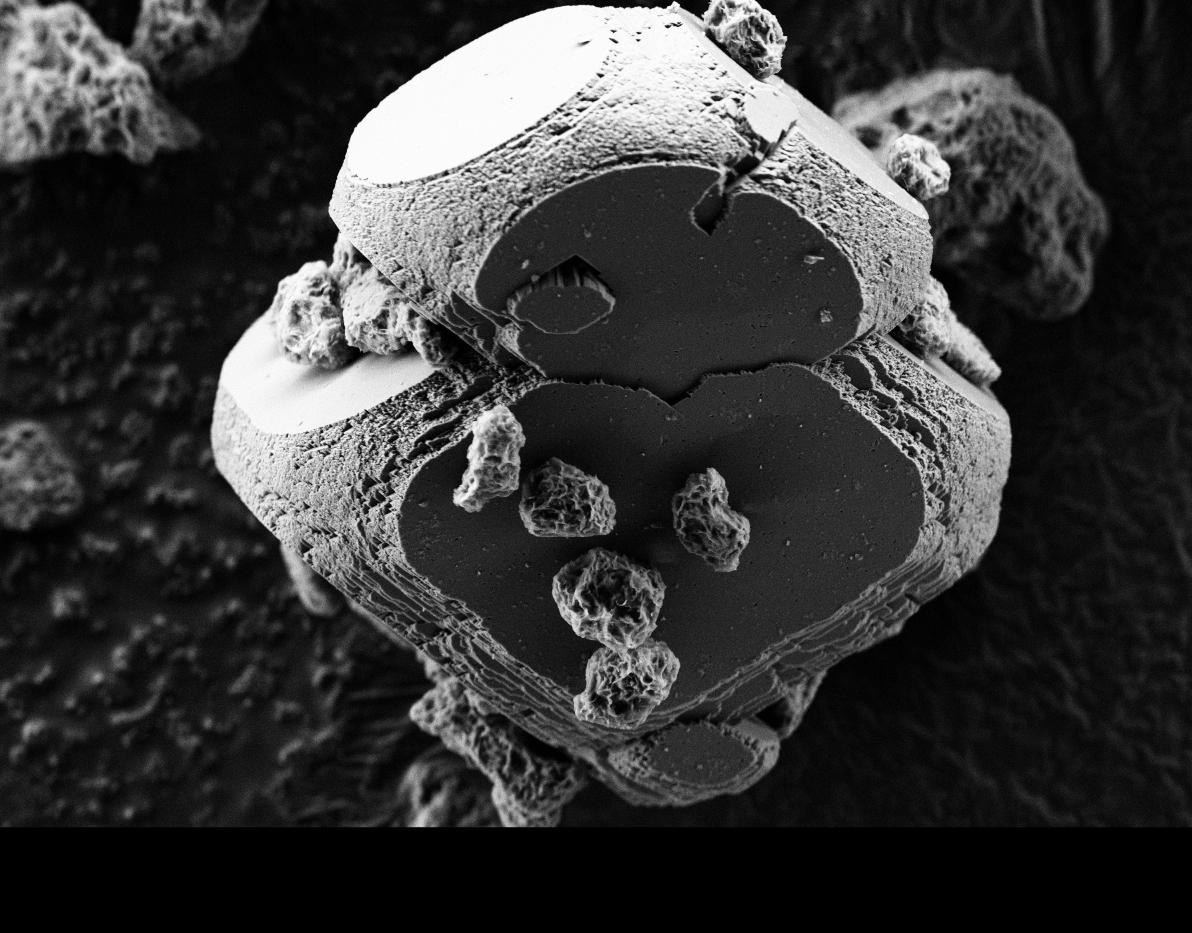
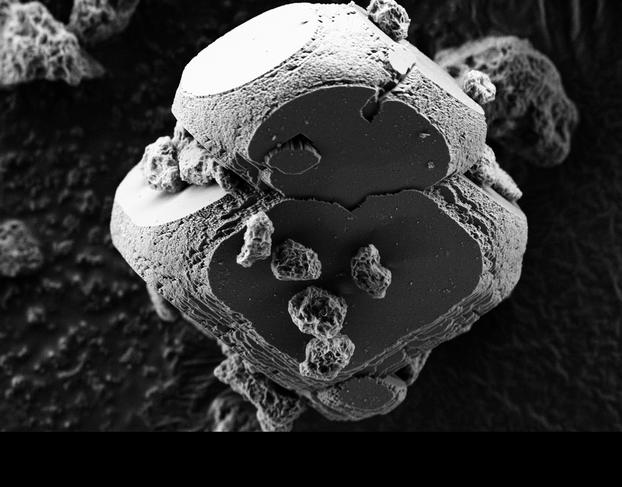
Créer de la roche en laboratoire, c’est le défi un peu fou que s’est lancé un consortium de recherche français, dans le cadre du projet Carmex. « Dans la nature, les roches sont lixiviées (lessivées) par l’eau de pluie et laissent s’échapper du calcium (Ca), mais aussi du fer (Fe) ou du magnésium (Mg) – autant de minéraux qui finissent dans les océans et les eaux souterraines explique Florent Bourgeois, du Laboratoire de génie chimique3, à Toulouse. Là, ils précipitent avec le CO2 dissous dans l’eau (sous sa forme d’ion CO3--) pour donner du carbonate de calcium ou calcite (CaCO3), du carbonate de fer ou sidérite (FeCO3), ou encore de la magnésite (MgCO3), sous la forme de minuscules résidus solides. »
L’idée des chercheurs est de reproduire, mais surtout d’accélérer ces processus géologiques naturels en chauffant le mélange. « Avec notre technique, on réussit à produire des “cailloux” d’une dizaine de microns, précise Florent Bourgeois. Mais pour cela, il faut porter la solution à 180 °C et appliquer une pression de quelques bars, des niveaux qui demandent encore trop d’apport énergétique et que nous nous employons à faire baisser. » Le stockage du CO2 sous forme solide n’est pas la seule finalité : « Les carbonates sont des matériaux qui entrent dans la fabrication du ciment, notamment. Ceux que nous fabriquons artificiellement pourraient eux aussi servir comme matériaux de construction », suggère le chercheur, qui rêve d’impliquer les professionnels de la construction dans son projet.
Reste à régler pour cela le seul vrai problème sur lequel les scientifiques n’ont pas la main : le prix de la tonne de carbone. Aujourd’hui, le carbone ne coûte pas plus de 8 à 10 euros la tonne, soit peu ou prou le prix de son extraction dans le sous-sol… « Il faudrait pour que la capture et la valorisation du CO2 deviennent intéressantes pour les industriels que le carbone avoisine les 80 euros la tonne », indique François Guyot. Il faudra patienter encore quelques années avant de rouler au CO2 atmosphérique ou d’habiter dans des tours construites grâce à celui-ci.
Voir aussi
Auteur
Journaliste scientifique, Laure Cailloce est rédactrice en chef adjointe de CNRS Le Journal et de la revue Carnets de science.