Vous êtes ici
L’astate, si rare et si précieux pour traiter le cancer
Une fois par mois, retrouvez sur notre site les Inédits du CNRS, des analyses scientifiques originales publiées en partenariat avec Libération.
Mendeleïev avait soupçonné son existence dès 1869. Dans son célèbre « Tableau périodique des éléments », il avait en effet prévu une case à remplir sous celle de l’iode... Ce n’est pourtant qu’en 1940 que l’astate (symbole At) a été officiellement découvert, après de nombreuses fausses annonces. Et pour cause : c’est l’un des éléments chimiques les plus énigmatiques.
La raison principale des mystères qui l’entourent encore aujourd’hui est son extrême rareté à l’état naturel. Issu de la désintégration d’éléments lourds tels que l’uranium, il est très instable et se désintègre à son tour en quelques heures seulement. À un instant T, on estime que seuls quelques grammes d’astate sont présents de façon transitoire sur la totalité de la croûte terrestre. Cela limite fortement les possibilités d’étude de ses caractéristiques, puisque seules des traces de cet élément peuvent être rassemblées. Il s’agit alors de quantités tellement infimes (de l’ordre du milliardième de gramme au mieux) qu’elles ne peuvent être directement observées, ni soumises aux instruments d’analyse habituellement utilisés pour caractériser les éléments chimiques.
Des radiations qui pénètrent faiblement dans la matière
Un isotope de ce radioélément intéresse pourtant la recherche médicale au plus haut point : l’astate-211. Lorsqu’il se désintègre, celui-ci libère en effet une particule radioactive possédant une énergie suffisante pour détruire les cellules qu’elle traverse, ce qui en fait un candidat sérieux à l’élimination de tumeurs cancéreuses aujourd’hui difficiles à soigner.
des particules
qui pourraient
permettre de
traiter des cellules
cancéreuses isolées.
Utiliser des isotopes radioactifs pour éliminer des tumeurs n’est pas nouveau : il existe déjà des thérapies employant cette approche. Cependant, les traitements actuels utilisent des éléments radioactifs émetteurs de particules « bêta », qui ont la propriété de pénétrer de plusieurs millimètres dans les tissus biologiques. Si elles sont utiles pour le traitement des tumeurs de taille importante (plusieurs millimètres de diamètre), ces particules se révèlent inopérantes pour le traitement des tumeurs de moins d’un millimètre, car elles détruisent également les tissus sains qui entourent la tumeur.
A contrario, l’astate-211 est un émetteur de particules « alpha » qui, en raison de leur faible pénétration dans la matière (l’épaisseur d’une feuille de papier, soit de 3 à 4 cellules à peine), pourraient permettre le traitement de cellules cancéreuses isolées (par exemple dans le cas de leucémies) ou de tumeurs de petite taille comme les micrométastases disséminées, et venir en complément de traitements conventionnels (chimiothérapie ou chirurgie) durant lesquels des résidus de tumeurs indétectables peuvent subsister et conduire à des rechutes.
Le recours aux sels d’iodonium, une piste prometteuse
L’astate-211, trop rare à l’état naturel pour un usage médical, peut aujourd’hui être produit artificiellement à l’aide d’accélérateurs de particules, comme le cyclotron Arronax, à Nantes, l’un des appareils les plus puissants au monde pour la production de radionucléides à visée médicale. Mais, pour le rendre utilisable en médecine, encore faut-il trouver le moyen de le transporter au plus près des cellules cancéreuses… Une nouvelle méthode chimique mise au point par le Centre de recherche en cancérologie Nantes-Angers1 et le National Cancer Institute (National Institutes of Health, États-Unis) pourrait enfin apporter la solution.
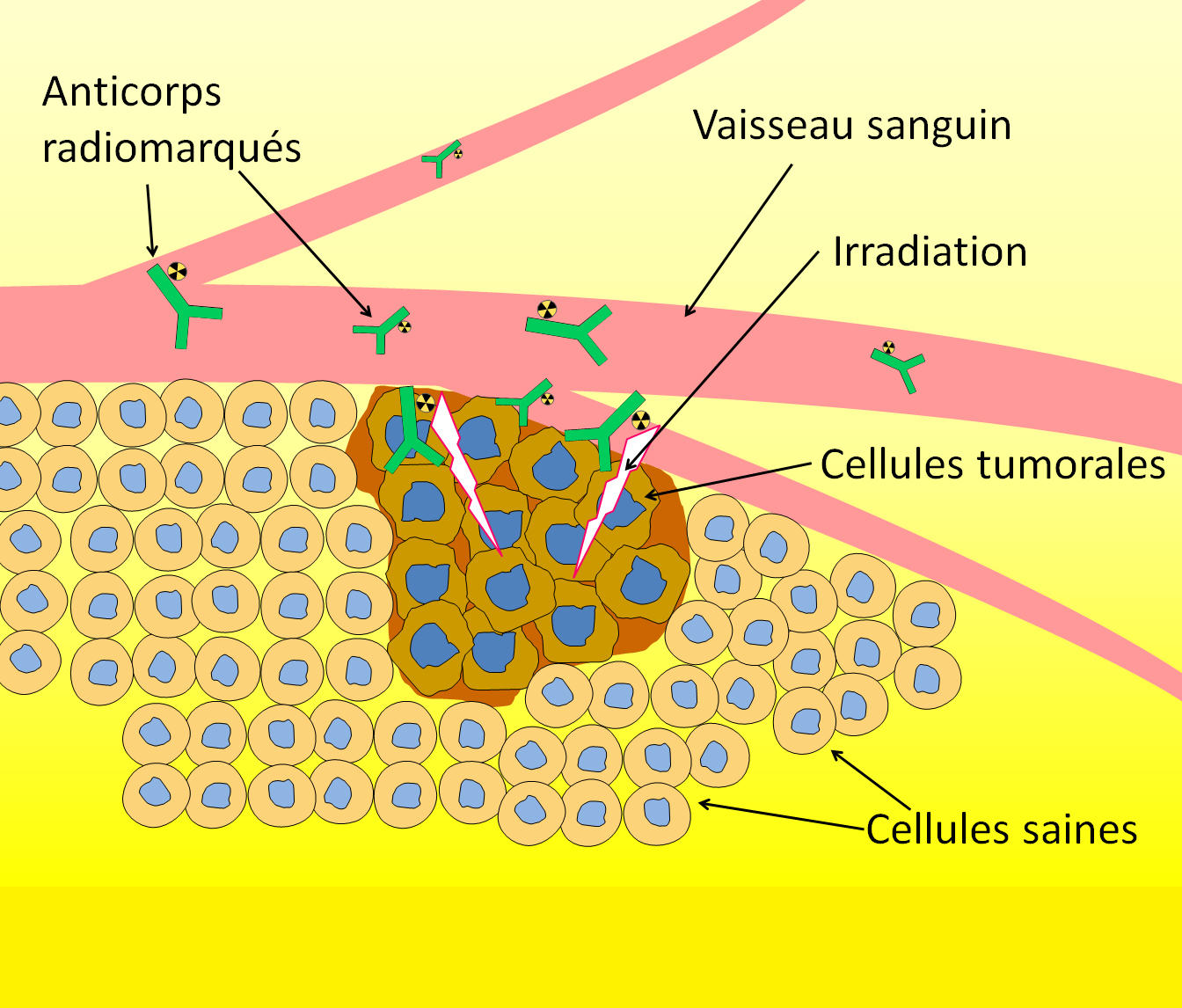
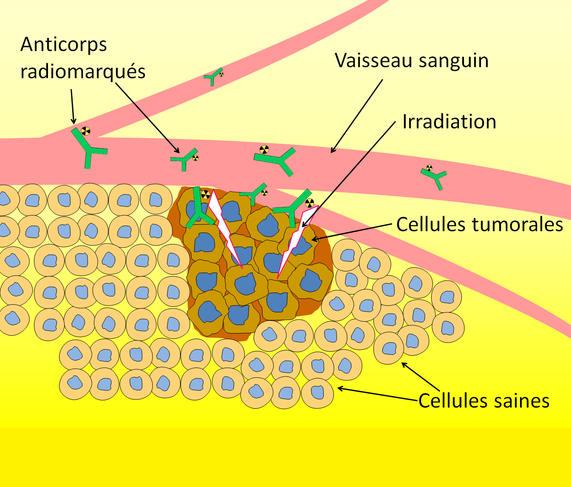
Pour transporter l’astate, la solution privilégiée par les chercheurs consiste à l’« accrocher » à une molécule capable de repérer les cellules tumorales. Les anticorps constituent aujourd’hui le véhicule privilégié par les chercheurs : issus du système immunitaire, ils sont capables de se fixer sur des antigènes bien identifiés que les cellules cancéreuses possèdent à leur surface. L’association anticorps-astate-211 peut ainsi être assimilée à un minuscule missile à tête chercheuse injecté au patient et destiné à déposer sa charge radioactive de façon très localisée au niveau de la tumeur, tout en limitant l’irradiation des tissus sains.

Mais, pour ne pas que la charge radioactive (l’astate-211) se dissocie du missile avant d’atteindre sa cible, il faut que ces deux éléments soient solidement accrochés. C’est désormais le cas grâce à de nouveaux composés, les sels d’iodonium : en les utilisant, l’opération de radiomarquage – c’est son nom – devient beaucoup plus efficace que les méthodes connues auparavant et surtout moins toxique pour l’organisme.
Publiés cet été dans la revue Chemistry-A European Journal 2, les résultats obtenus à Nantes permettent d’envisager sérieusement une utilisation prochaine de l’astate-211 en clinique. L’étude clinique, promue par le CHU de Nantes, sera menée en collaboration avec l’Institut de cancérologie de l’Ouest dans le cadre d’un vaste programme de recherche autour du cyclotron Arronax et du Centre de recherche en cancérologie Nantes-Angers.
Les points de vue, les opinions et les analyses publiés dans cette rubrique n’engagent que leur auteur. Ils ne sauraient constituer une quelconque position du CNRS.
- 1. Unité CNRS/Inserm/Univ. de Nantes/Univ. d’Angers.
- 2. Chem. Eur. J., 22 août 2016, vol. 22 (35). DOI: 10.1002/chem.201600922 http://onlinelibrary.wiley.com/doi/10.1002/chem.201600922/full