Vous êtes ici
Les 9 questions clés de la médecine prédictive (partie 1)
Temps de lecture : 9 minutes
1) Que nous apprennent les tests génétiques ?
L’analyse de nos gènesFermerUn gène est un fragment d'ADN qui contient de quelques milliers de lettres à plus de 2 millions. Il y a 30 000 gènes dans notre ADN. Si une ou deux lettres d'un gène sont différentes par rapport à la version normale, on dit qu'il a muté. Il peut alors provoquer une maladie génétique. (dans le sang, la salive, etc.) permet le diagnostic de 1 000 maladies génétiques (sur les 5 000 répertoriées) et l’estimation de la susceptibilité à des centaines d’autres influencées par la génétique. Ces tests indiquent des facteurs de risque sous forme de pourcentages. C’est un calcul de probabilité, celle de développer une maladie si nous avons telle variation d’un gène, par comparaison à la population qui ne l’a pas. « Le calcul, réalisé à partir de statistiques d’épidémiologie, tient aussi compte des variabilités selon les groupes géographiques, l’âge, etc. », explique Anne Cambon-Thomsen, généticienne1 au CNRS. Les chiffres peuvent donc varier pour une même pathologie. Par exemple, selon l’Institut national du cancer, une mutation du gène BRCA1 implique de 51 à 75 % de risque de développer un cancer du sein héréditaire avant 70 ans, contre environ 10 % dans la population générale (tous cancers du sein confondus, héréditaires ou non). Et le risque d’être atteint de dégénérescence maculaire liée à l’âge (DMLA) est 2,5 fois plus élevé quand on est porteur d’une variation du gène CFH. Ce type de risque devient une certitude pour certaines maladies génétiques comme la maladie de Huntington, dégénérescence du système nerveux central inéluctable vers l’âge de 40 ans si on a le gène HD muté. Mais la plupart des maladies sont multifactorielles. Les gènes, lorsqu’ils sont impliqués, n’entraînent alors que des risques faibles qui se mêlent à de nombreux autres facteurs comme l’alimentation, la rencontre avec un virus, une bactérie, etc. « Ainsi, posséder le variant génétique qui rend moins résistant à la lèpre ne vous fera en réalité pas courir plus de risques que votre voisin de pallier si vous vous trouvez dans une région préservée de l’agent infectieux de cette maladie… », commente Anne Cambon-Thomsen. Autre exemple : le diabète de type 2 est autant lié à des gènes qu’à la consommation de sucre et à un mode de vie trop sédentaire.
2) Prédire permettra-t-il de guérir ?
Ce n’est pas si simple. En ce qui concerne les maladies génétiques comme Huntington, certains cancers héréditaires ou la mucoviscidose, la thérapie géniqueFermerMéthode consistant à introduire des gènes dans les cellules d’un organisme pour y corriger une anomalie. pourrait permettre, en théorie, de guérir avant même d’être malade. « Mais cette technique n’a encore donné que peu de résultats probants », rappelle Hervé Chneiweiss, directeur de recherche au CNRS, directeur de l’unité Plasticité gliale et président du comité d’éthique de l’Inserm. En revanche, la chirurgie préventive permet bel et bien de supprimer un risque s’il concerne un organe précis et amputable, comme le sein ou les ovaires. Bien entendu, de telles opérations confrontent médecins et patients à des décisions extrêmement difficiles, dans la mesure où une part non négligeable des individus peut ne jamais développer la maladie. Autre approche : prescrire une surveillance accrue en cas de forte prédisposition. « À condition que le dépistage soit inoffensif. La question se pose par exemple pour les rayons X des mammographies : ceux-ci sont susceptibles de provoquer des lésions dans l’ADN et de favoriser justement les cancers du sein héréditaires que l’on guette », pointe Hervé Chneiweiss. Enfin, du côté des maladies multifactorielles, associées à de faibles risques, « la prédiction par les gènes n’a aujourd’hui que peu d’intérêt médical », résume Anne Cambon-Thomsen. Sauf peut-être à pousser les gens à faire du sport, à manger moins de sucre et à prendre d’autres bonnes résolutions en cas de prédisposition au diabète, à des maladies cardiovasculaires, etc. « Reste à prouver que l’information génétique influence davantage les gens que les campagnes de prévention destinées à l’ensemble de la population, ce que les études de comportement actuelles peinent à démontrer », commente la chercheuse.
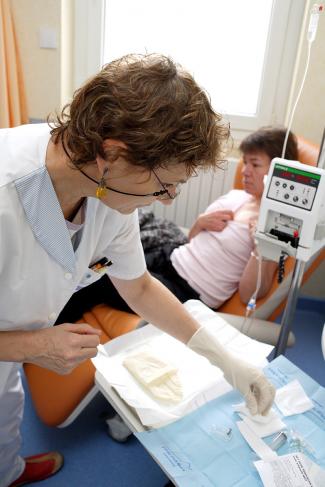
3) Peut-on personnaliser les traitements en fonction de l’ADN des patients ?
Oui, car on peut aujourd’hui prédire l’efficacité de certains traitements en fonction de l’ADN du patient. « Cette branche de la médecine, la pharmacogénétique, est en plein essor », informe Anne Cambon-Thomsen. L’intérêt est inestimable : éviter d’administrer des médicaments inefficaces et supprimer des effets secondaires désagréables, voire mortels. De nombreux exemples affichent déjà des résultats tangibles. L’Agence européenne du médicament recommande ainsi, depuis 2008, un test génétique avant la prise d’Abacavir (un anti-VIH) afin d’identifier les patients porteurs d’un variant d’un gène HLA. Selon les études épidémiologiques, la moitié d’entre eux tolèrent en effet très mal ce médicament, voire en meurent. « Mais c’est probablement en cancérologie que la génomique suscite aujourd’hui le plus d’applications », poursuit Anne Cambon-Thomsen. Celle-ci permet en effet d’améliorer le diagnostic et de décider de la chimiothérapie la plus adéquate en fonction des altérations génétiques identifiées dans la tumeur, notamment pour les cancers du sein.
4) Quels sont les grands progrès attendus de la génomique ?
En plus de faciliter le choix des traitements, la génomique sert aussi à en mettre au point de nouveaux. « Cette approche permet en effet d’identifier de nouvelles cibles liées à des mutations génétiques sur lesquelles pourront agir de nouvelles molécules médicamenteuses à développer », commente Anne Cambon-Thomsen. Souvent, ces mutations ne concernent qu’une partie seulement des patients, d’où une médecine de plus en plus personnalisée. Une mutation du gène CFTR vient ainsi de permettre la mise au point du premier médicament contre la mucoviscidose, l’Ivacaftor, très efficace, mais chez 5 % des malades seulement. « Et, dans le domaine du cancer, des recherches visent maintenant à comparer l’ensemble du génome de la tumeur avec celui de tissu sain de l’individu. Le but serait à l’avenir de traiter cette pathologie selon le profil génétique de la tumeur et du patient », explique la chercheuse. Et pour l’avenir plus lointain ? « La médecine passera par la recherche des interactions entre les gènes, encore très peu étudiées, et des interactions des gènes avec l’environnement, pour lesquelles il faudra développer les cohortesFermerEnsemble d’individus suivis pour une durée définie dans le cadre d’une étude épidémiologique. avec des données sur les modes de vie des individus », conclut Anne Cambon-Thomsen.
5) Qui peut faire un test génétique ?
En pratique, tout le monde. Il suffit en effet d’expédier sous pli un peu de salive à un laboratoire étranger accessible sur Internet. Le kit vendu par 23andMe, par exemple, permettait de connaître sa susceptibilité génétique à développer 162 maladies et à réagir à 20 médicaments, le tout pour une centaine de dollars2. « Mais en France, obtenir ainsi un tel test est illégal », commente Sonia Desmoulin-Canselier, chercheuse à l’Unité mixte de recherche de droit comparé, à Paris3. La loi relative à la bioéthique fixe un cadre très strict : un test ne doit être entrepris que dans un but judiciaire, pour la recherche scientifique ou dans un but médical. Il peut alors s’agir de confirmer le diagnostic d’un patient présentant les symptômes d’une maladie génétique, de rechercher une maladie héréditaire en l’absence de symptômes, de permettre un choix éclairé en matière de procréation, etc. Les praticiens qui font les analyses doivent avoir un agrément de l’Agence de la biomédecine. Les tests doivent être prescrits par un médecin qui doit recueillir le consentement signé du patient, ou bien de ses parents s’il s’agit d’une personne mineure. « Dans ce dernier cas, il faut impérativement que le patient ou sa famille tire un bénéfice médical du test, c’est-à-dire des mesures préventives ou curatives immédiates », souligne Simone Bateman, sociologue au Cermes34. L’accompagnement du patient par un conseiller en génétique et des psychologues lors du protocole est capital étant donné l’angoisse et les mauvaises interprétations que les résultats peuvent causer. Les tests Internet, outre une fiabilité parfois controversée, n’offrent souvent aucun suivi de ce type.
À lire aussi :
Les 9 questions clés de la médecine prédictive (partie 2)
Le dépistage prénatal : jusqu'où aller ?
La médecine prédictive, médecine d'avenir ?
- 1. Dans l’unité Épidémiologie et analyses en santé publique : risques, maladies chroniques et handicaps (Inserm/Univ. de Toulouse/UPS).
- 2. Depuis décembre 2013, la Food and drug administration (FDA) a interdit à la société 23andMe de produire des tests génétiques relatifs à la santé. La FDA met essentiellement en doute la valeur des conseils de santé proposés par la société sur son site Web.
- 3. Unité CNRS/Univ. Paris-I Panthéon-Sorbonne.
- 4. entre de recherche, médecine, sciences, santé, santé mentale, société (CNRS/Inserm/EHESS/Univ. Paris-Descartes).
Voir aussi
Auteur
Journaliste scientifique, autrice jeunesse et directrice de collection (une vingtaine de livres publiés chez Fleurus, Mango et Millepages).
Formation initiale : DEA de mécanique des fluides + diplômes en journalisme à Paris 7 et au CFPJ.
Plus récemment : des masterclass et des stages en écriture...