Vous êtes ici
Quel vaccin contre le Covid-19 ?
Alors que l’épidémie de Covid-19 semble partie pour durer, et à défaut de traitement efficace, la mise au point d’un vaccin pour protéger la population mondiale apparaît comme la meilleure option à ce jour. Tous les laboratoires, privés comme publics, y travaillent d’arrache-pied : près de 180 candidats-vaccins contre le Covid-19 sont ainsi en développement, dont une quarantaine ont atteint la phase d’essais cliniques chez l'humain, plus ou moins avancée. Sur ces quarante candidats, dix sont entrés dans la 3e et dernière étape - parmi eux, le vaccin à ARN de l'américain Pfizer (allié à l'entreprise allemande de biotechnologie BioNTech) qui affole l'actualité ces jours-ci.
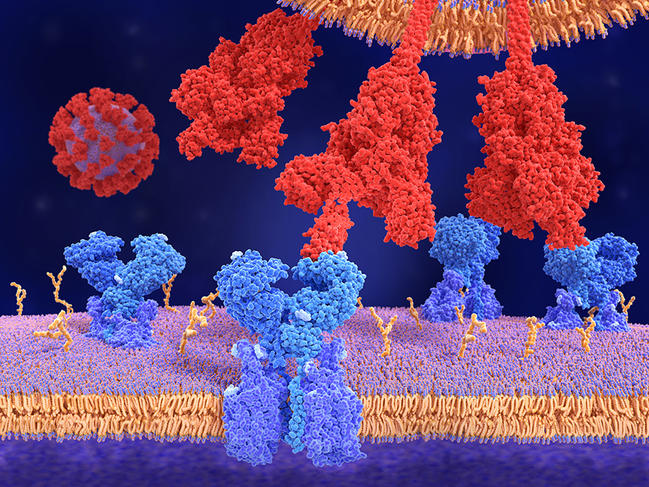
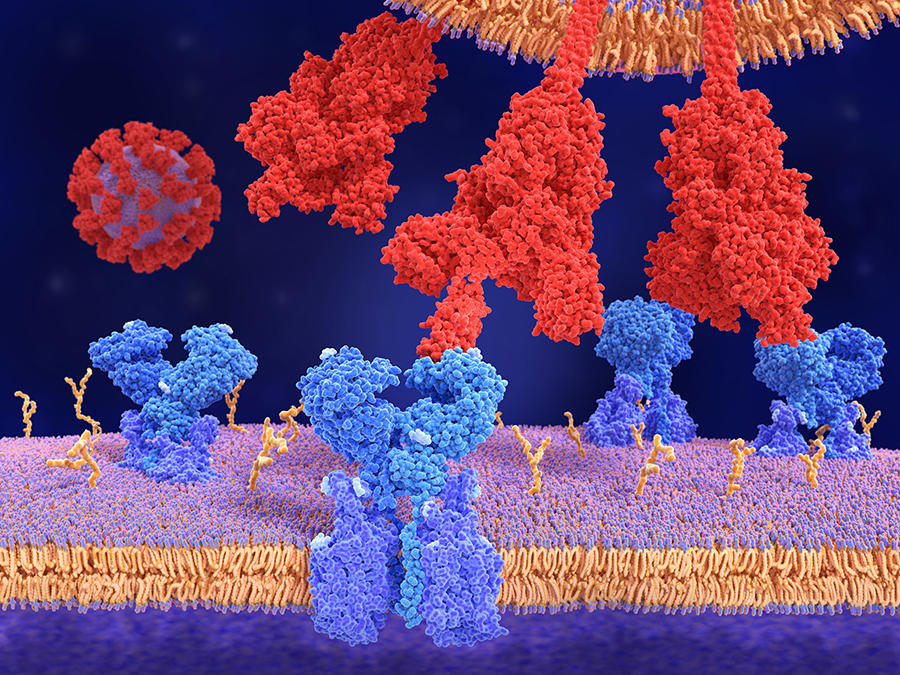
Le principe de la vaccination est toujours le même : il s’agit de présenter un pathogène (virus, mais aussi parasite ou bactérie) à notre système immunitaire afin qu’il apprenne à le reconnaître et à fabriquer des anticorps spécifiques qui seront prêts à le neutraliser lorsque nous le rencontrerons dans la vraie vie. « En réalité ce n’est pas le pathogène en tant que tel qui déclenche la réponse immunitaire, mais des protéines bien particulières qui se trouvent à la surface du virus, les antigènes, explique Bruno Pitard, physico-chimiste au Centre de recherche en cancérologie et immunologie Nantes-Angers1. Ces antigènes sont la clé qui permet au virus de pénétrer dans la cellule, qu’il va alors mettre à son service pour se reproduire. Concernant les coronavirus, l’antigène le mieux reconnu est la protéine « S » (pour Spike), cette protéine en forme de pique qui donne au virus son aspect « hérissé » si particulier.
L’idée du vaccin est évidemment d’inoculer le pathogène sous une forme totalement inoffensive, qui ne risque pas de déclencher la maladie contre laquelle il prétend nous défendre. Plusieurs techniques sont possibles pour cela – des techniques éprouvées comme l’utilisation du virus entier rendu inoffensif, aux techniques plus récentes comme les vaccins à ADN ou ARN. Toutes ces pistes sont actuellement exploitées dans la recherche d’un vaccin contre le Covid-19.
► Quelles sont les techniques utilisées ?
Le virus entier, atténué ou inactivé
La première technique, utilisée depuis que la vaccination existe, consiste à présenter le virus entier au système immunitaire, ce qui suppose de le cultiver en très grande quantité. C’est la voie suivie notamment par plusieurs laboratoires chinois pour la mise au point d’un vaccin anti-Covid. Pour s’assurer que le vaccin sera sans danger pour le corps, on peut soit présenter le virus sous une forme inactivée (tuée), après l’avoir préalablement chauffé ou passé au formol – c’est la technique de Pasteur –, soit le présenter sous une forme atténuée. Dans ce second cas, le virus est toujours vivant mais a perdu sa dangerosité. « C’est de la sélection génétique. On ne garde que les souches virales qui ont acquis des mutations qui ne donnent pas la maladie », explique Frédéric Tangy, virologiste, directeur du Laboratoire d’innovation vaccinale de l’Institut Pasteur. De nombreux vaccins ont été développés sur ce modèle (rubéole, fièvre jaune, rougeole…).
Dans le cas d’un virus inactivé, le virus est mort et a perdu le pouvoir de se répliquer dans l’organisme, il faut généralement faire des rappels pour qu’il soit efficace. Dans le cas du virus atténué, le virus est vivant et a gardé sa capacité à se multiplier dans l’organisme, une seule injection suffit en général. Inconvénient des vaccins utilisant des virus entiers : il existe un risque statistique, impossible à éliminer totalement, qu’une infime proportion de particules virales gardent leur capacité à infecter l’individu. Autre inconvénient, propre aux vaccins inactivés (tués) : celui d’altérer la conformation (la forme) de la protéine S, ce qui pourrait rendre le vaccin moins efficace selon Bruno Pitard.
Un morceau de virus
Deuxième possibilité : au lieu de présenter le virus entier au système immunitaire, on se concentre sur l’antigène qui provoque la réponse immunitaire. Aucun risque de développer la maladie, dans ce cas. « L’idée ici est de faire produire la protéine Spike en usine par des lignées cellulaires de mammifères et de l’introduire dans l’organisme en association avec un adjuvant qui donnera le signal d’alerte au système immunitaire, explique Bruno Pitard. Seule, une protéine, même s’il s’agit d’une protéine virale, ne sera pas considérée comme dangereuse par le corps qui en produit lui-même des milliards. »
L’association adjuvant-antigène, au contraire, est immédiatement reconnue comme un corps étranger : les macrophages, la première ligne de défense du système immunitaire qui patrouille en permanence dans le corps, vont le « manger » et identifier « S » comme une protéine exogène. La production d’anticorps est alors lancée. Les vaccins contre l’hépatite B et le papillomavirus sont fabriqués suivant cette technique, choisie par le laboratoire Sanofi (allié pour l’occasion au laboratoire GlaxoSmithKline) pour son vaccin anti-Covid.
Les vaccins à ADN/ARN
Puisqu’il est établi que le rôle de la protéine Spike, protéine en forme de « pique » du coronavirus, est crucial dans le déclenchement de la réponse immunitaire neutralisante du Covid-19, pourquoi ne pas la faire produire directement par le corps humain, en introduisant dans nos cellules la séquence génétique qui code pour la fabrication de cette protéine virale ? Cela évite d’injecter des particules de Covid-19 entières dans le corps ou d’utiliser des adjuvants. Problème, l’ADN ou l’ARN sont dégradés par nos enzymes à peine entrés dans l’organisme. Pour s’assurer que le code de la protéine Spike arrive intact jusqu’à l’intérieur de nos cellules, il lui faut un véhicule capable de l’y transporter : or quoi de mieux qu’un virus pour faire le travail ?
Deux possibilités s’offrent aux scientifiques. Soit fabriquer un virus « canada dry », selon l’expression de Bruno Pitard – une enveloppe totalement artificielle composée de molécules mimant les lipides et les protéines, qui aura tous les attributs d’un virus sans en être un. C’est l’option prise par le laboratoire Pfizer allié à BioNTech, ou enocre par l’entreprise de biotechnologie Moderna Therapeutics. Soit utiliser un virus bien réel, mais inoffensif pour nous.
« L’utilisation de vecteurs viraux – de vrais virus donc – est la stratégie pour laquelle de nombreux laboratoires ont opté pour le développement de leur vaccin anti-Covid, explique Frédéric Tangy. Deux types de plateformes virales sont utilisées à cet effet : des adénovirus, qui ne sont rien d’autre que des virus du rhume (c’est le choix fait par les chercheurs russes qui développent le vaccin Spoutnik V), ou le vaccin de la rougeole, utilisé depuis quarante ans pour vacciner les enfants, et dont l’ARN est modifié afin d’y intégrer le code de la protéine Spike. C’est cette plateforme rougeole que nous avons choisie à Pasteur pour développer notre candidat-vaccin contre le Covid-19. »
Avec une incertitude soulevée par Bruno Pitard : quid du cas de figure où la personne vaccinée aurait déjà des anticorps contre le virus utilisé comme « vecteur » ? C’est pour éviter ce possible écueil que le laboratoire AstraZeneca, associé à l’université d’Oxford, a fait le choix d’utiliser un adénovirus modifié de... chimpanzé. « D’après nos essais cliniques déjà réalisés avec le vecteur rougeole, cette pré-immunité ne semble pas poser de problème », indique pour sa part Frédéric Tangy.
Le déploiement de vaccins génétiques à grande échelle serait une première. Si dans la décennie qui vient de s’écouler, plusieurs candidats-vaccins utilisant ces nouvelles technologies sont arrivés jusqu’à la phase 3 des essais cliniques chez les humains (dont un candidat-vaccin contre Ebola), aucun vaccin à ADN/ARN n’a encore été déployé en médecine humaine à ce jour, et les scientifiques reconnaissent manquer encore de recul sur leur utilisation. « Ce n’est pas un saut dans l’inconnu, tempère néanmoins Bruno Pitard. Des vaccins à ADN sont en effet utilisés depuis plusieurs années pour prévenir l’apparition de certaines pathologies chez des animaux comme le cheval, le poisson d’élevage ou encore le chien. »

► Quand saura-t-on si les vaccins actuellement en développement sont efficaces ?
Au vu de la gravité de la pandémie, l’organisation mondiale de la santé (OMS) a fixé à 50 % le seuil d’efficacité requis pour mettre sur le marché un vaccin anti-Covid-19 – c’est un seuil proche du vaccin contre la grippe, très inférieur néanmoins aux performances de la plupart des vaccins aujourd’hui utilisés chez les humains. À ce jour, près d’une quarantaine de candidats-vaccins ont passé le stade des essais précliniques menés chez l’animal, et sont aujourd’hui en phase clinique chez l'humain. Parmi eux, dix sont entrés en phase 3 – la dernière, mais aussi la plus longue phase des essais cliniques.
Un calendrier accéléré
Pour rappel, les essais cliniques comportent trois étapes. La première, menée sur quelques dizaines de volontaires, permet de s’assurer que le vaccin est sûr et n’entraîne pas d’effets secondaires sévères. La deuxième phase clinique, conduite sur un échantillon plus large (environ 200 personnes), permet de vérifier que les personnes vaccinées produisent bien les anticorps recherchés pour lutter contre la maladie. La -troisième phase, menée généralement sur 30 000 à 50 000 personnes au minimum (soit plusieurs années d'observation, en temps normal), fait la preuve de l’efficacité du vaccin sur le terrain, grâce à un système de tests en double aveugle.
« Les essais de phase 3 sont effectués dans des zones de forte circulation du virus, détaille Frédéric Tangy. Un groupe est vacciné avec le candidat-vaccin, tandis que le second groupe reçoit un placebo. Selon les critères fixés par l’OMS, le vaccin contre le Covid sera jugé efficace si parmi les personnes ayant reçu le produit, on compte 50 % d’infections en moins que dans le groupe témoin. » Vu l’urgence de la situation sanitaire, des autorisations dérogatoires de mise sur le marché pourraient être accordées au vaccin qui obtient de bons résultats alors que la phase 3 est toujours en cours… En laissant encore en suspens de nombreuses questions sur le virus.
.

La délicate question des anticorps
La principale interrogation concerne les anticorps produits après la vaccination. Combien de temps seront-ils présents dans le sang, alors que plusieurs études scientifiques font état de leur disparition au bout de quelques semaines à quelques mois chez des malades confrontés une première fois au Covid-19 ? « La présence d’anticorps dans le sang, mesurée par une sérologie, n’est pas la seule réponse du système immunitaire, nuance Claude-Agnès Reynaud, immunologiste à l’hôpital Necker-Enfants malades2. La mémoire immunitaire joue également un rôle crucial pour une protection sur la durée. Ces cellules-mémoire (des lymphocytes B) produites dans la moelle osseuse peuvent se réactiver en cas de nouvelle infection et fabriquer à nouveau des anticorps. Ainsi, une personne peut très bien être séronégative et avoir des B-mémoire. » Or ces cellules-mémoire ne sont pas mesurées lors des essais cliniques – seuls les laboratoires de recherche fondamentale sont équipés pour cela.
Autre question épineuse, celle des anticorps dits « facilitants ». Il arrive en effet que les anticorps produits ne soient pas assez fonctionnels et aient un effet délétère en cas de nouvelle infection – en clair, qu’ils aggravent la maladie au lieu de la combattre. « C’est un phénomène observé avec la dengue, auquel s’est heurté un candidat-vaccin développé contre cette maladie, ou encore avec le virus de la bronchiolite du nourrisson, rappelle Frédéric Tangy. En 2008, le développement d’un vaccin contre le sida a dû être interrompu en phase 3 pour les mêmes raisons. »
Rien n’est décidément simple en matière de vaccinologie... « La recherche, c’est le temps long. Ici, dans le labo, on change d’avis tous les jours sur le Covid », rappelle Claude-Agnès Reynaud, qui affirme pourtant rester une « irrémédiable optimiste ». « Sur le papier, le Covid est un virus assez “bête”. Il varie peu, notamment dans la façon dont il infecte la cellule ; la plupart des gens font une bonne réponse et développent des anticorps neutralisants facilement. Pourquoi, dans ces conditions, n’arriverait-on pas à développer un vaccin qui fonctionne ? » ♦
À lire :
Covid-19: la recherche mobilisée
Voir aussi
Auteur
Journaliste scientifique, Laure Cailloce est rédactrice en chef adjointe de CNRS Le Journal et de la revue Carnets de science.