Vous êtes ici
Covid-19 : « L’évolution virale reste largement imprévisible »
La vague Omicron semble passée et l’actualité est de plus en plus prise par la guerre en Ukraine. Mais où en sommes-nous vraiment au niveau des variants et de l’épidémie de Covid-19 ?
Samuel Alizon1. Notre perception de l’épidémie est trop facilement influencée par ses tendances en France : le tableau devient très noir quand elle croît, puis tout paraît rose quand elle décroît. Cette réaction existe même chez les chercheurs, mais méfions-nous en. À l’international, nous voyons bien que la situation n’est pas synchronisée, avec notamment une vague du variant Omicron qui cause beaucoup de décès en Asie du Sud-Est. Nous devons donc garder à l’esprit que les pandémies fonctionnent sur un temps long et que les hétérogénéités locales sont fortes. Bref, il ne faut pas trop extrapoler à partir du contexte actuel dans un pays donné.

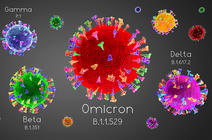
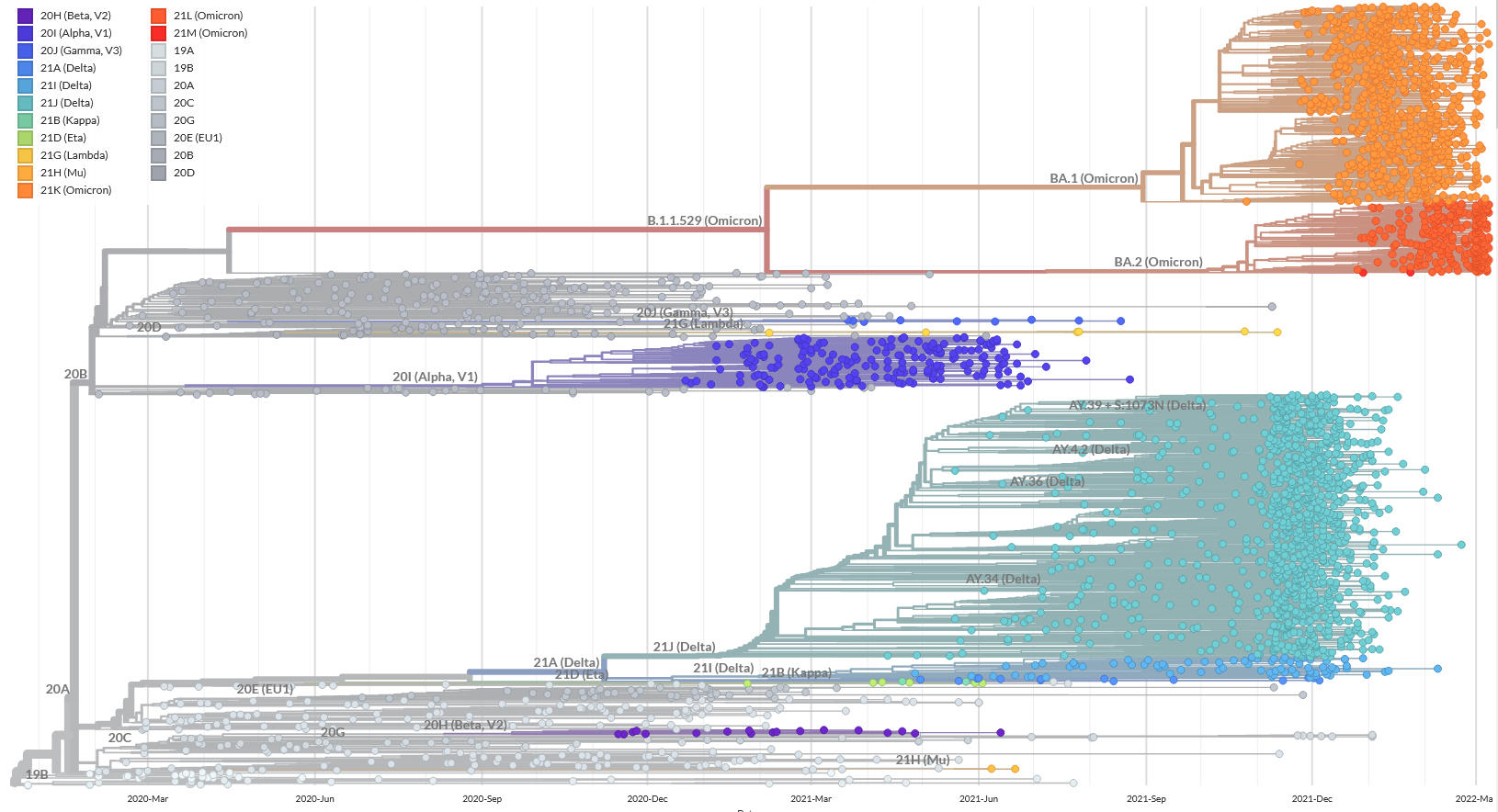
Ceci dit, à ce jour (l’entretien a été réalisé le 8 mars, Ndlr), le variant BA.2 est clairement majoritaire en France. Il s’agit d’une lignée sœur de BA.1, la lignée d’Omicron qui a causé la vague de janvier. Toutes deux auraient divergé il y a environ un an en Afrique australe. BA.2 est aussi différent de BA.1 que le variant Delta l’est de l’Alpha, mais partage certaines de ses caractéristiques : environ deux fois plus contagieux et trois fois moins virulent que Delta dans une population vaccinée. Les raisons de ce remplacement sont débattues, mais, selon nos collègues britanniques, il pourrait s’agir d’une question de temporalité, les infections BA.2 étant contagieuses un peu plus rapidement. On ne sait cependant pas quelle sera l’ampleur de son pic épidémique, car, outre la biologie, la politique et les comportements individuels jouent un rôle important.
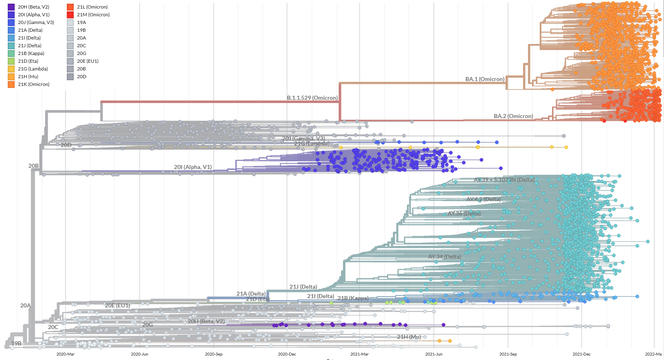
Même si des tendances de fond se dégagent, l’évolution des variants reste largement imprévisible. Le variant Alpha est apparu alors que la plupart des épidémiologistes pensaient que l’évolution du SARS-CoV-2 n’était que neutre. Au moment où on craignait de voir émerger des mutants de variant Alpha échappant à l’immunité, Delta est survenu et l’a remplacé. Et quand la surveillance s’est concentrée sur des clusters de Delta portant des mutations inquiétantes, Omicron l’a supplanté encore plus rapidement. Toutefois, Omicron marque une rupture, au point qu’on se demande si nous ne sommes pas en train de vivre un branchement évolutif, c’est-à-dire un passage d’une espèce à deux espèces différentes.
En effet, les virus des lignées Omicron semblent exploiter une niche écologique différente des autres variants du SARS-CoV-2, qui infectent les voies respiratoires basses. Omicron s’en prend plutôt aux voies respiratoires hautes, où la réponse immunitaire est moins importante. Nous ne savons pas dans quelle mesure ces deux types de variants coexisteront, avec chacun sa cible de prédilection dans notre organisme, ou si BA.2 deviendra hégémonique.

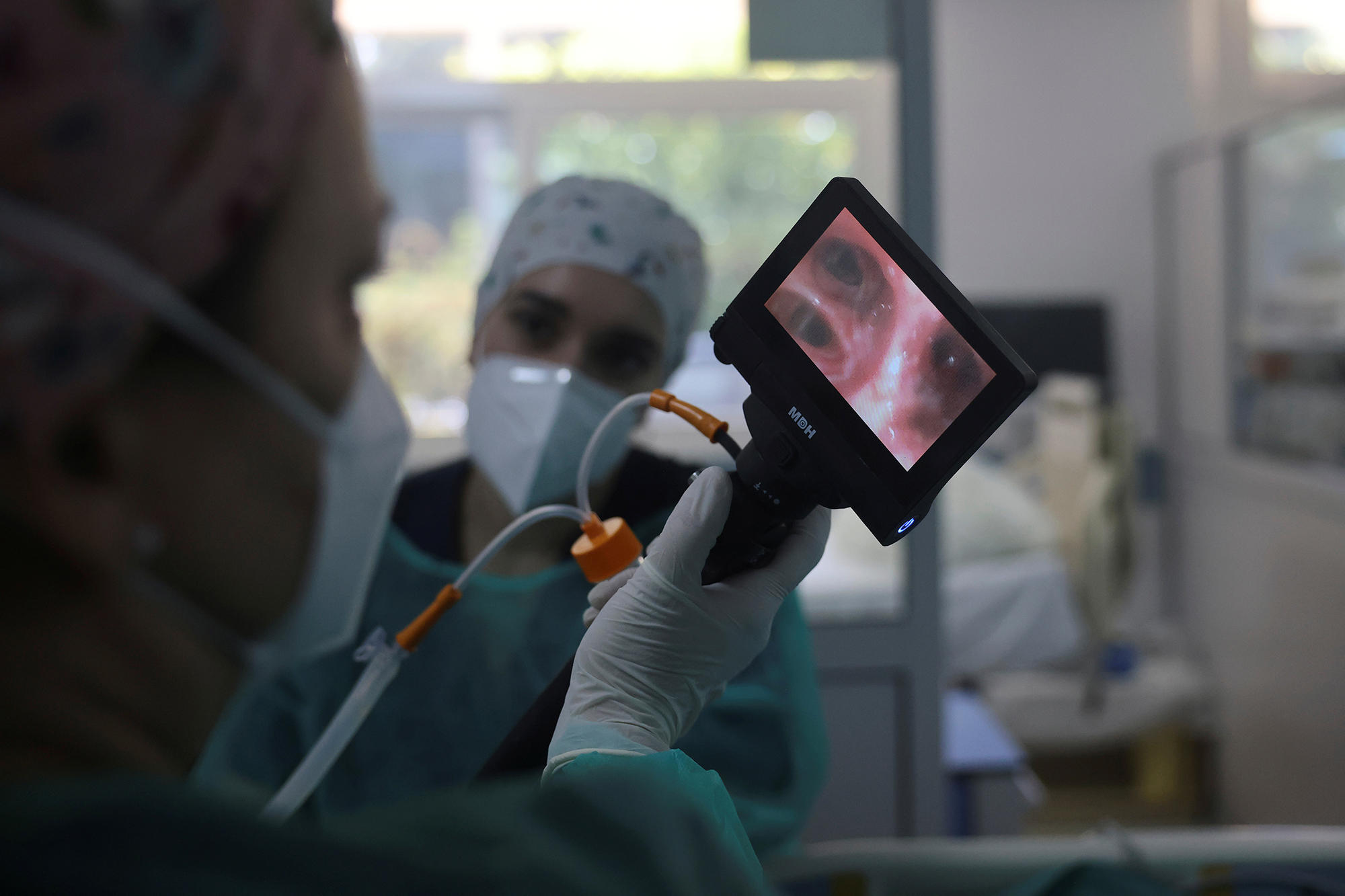
Quelles sont les possibilités décrites par la recherche ?
S. A. Le Royaume-Uni est très en avance sur ces questions et a publié, en février 2022, un rapport comprenant quatre scénarios d’évolution de l’épidémie sur le long terme, donc à un horizon de plus de 18 mois. L’un est optimiste, deux sont considérés comme médians et le quatrième est au contraire pessimiste. La projection optimiste correspond au prolongement de l’état actuel en Europe, où le virus présente un échappement immunitaire faible et une sévérité d’infection limitée grâce à la vaccination et aux traitements. Si, dans ce scénario, les vagues hivernales demeurent possibles, leur ampleur serait limitée et les rappels vaccinaux ne concerneraient que les personnes à risque.
L’échappement immunitaire serait plus prononcé dans les scénarios médians, ce qui provoquerait de nouvelles vagues d’ampleur, potentiellement dès l’automne. On connaît encore assez mal les propriétés de l’immunité sur le long terme, mais les données britanniques, là encore, indiquent que la protection est moins durable contre Omicron que contre Delta. Par conséquent, ces scénarios pourraient nécessiter, certaines années, de nouvelles campagnes de vaccination générales.
Enfin, dans le pire des scénarios, non seulement l’immunité serait faible, mais la sévérité de l’infection serait accrue, par exemple du fait de l’émergence d’un nouveau variant ou de la généralisation de résistances virales aux traitements. Il faudrait alors mettre la composition des vaccins à jour ou recourir aux interventions non pharmaceutiques. Aujourd’hui, difficile d’avoir des certitudes à plus de quelques mois et nous nous contentons de cerner le champ des possibles. Au vu des modélisations de notre équipe, à moyen terme, les deux scénarios extrêmes semblent peu probables, mais, encore une fois, les variants démontrent que des événements rares peuvent avoir des conséquences planétaires.
Comment est organisé le suivi des variants ?
S. A. Là encore, les Britanniques ont incontestablement un temps d’avance en termes de qualité de suivi et d’analyse. Mais surveiller l’apparition de nouveaux variants nécessite une excellente connaissance du terrain. Au niveau international, cela signifie donc de faire confiance aux épidémiologistes de chaque pays. C’est ce qu’il s’est passé avec Omicron en Afrique du Sud, où les chercheurs ont partagé leur inquiétude avec le reste du monde quand ils ont vu que dans plusieurs provinces l’épidémie, avec toutes ses spécificités locales, ne se comportait plus de la même manière.
Classiquement, la détection et le suivi des variants préoccupants reposent sur trois critères : épidémiologiques, pathologiques, et génétiques. Généralement, on constate d’abord des clusters ou des croissances localisées de l’épidémie, à contre-courant avec la tendance de fond. Les études de terrains couplées au séquençage des génomes viraux montrent ensuite que ces rebonds sont provoqués par une lignée spécifique qui cause des symptômes différents, que ce soit en termes d’échappement immunitaire, de contagiosité ou de virulence. La France a rapidement mis en place un réseau épidémiologique pour la surveillance de ces critères. Malheureusement, nous sommes vraiment dans une position de spectateurs par rapport au Royaume-Uni, notamment sur l’analyse des variations de sévérité ou d’échappement immunitaire. Toutefois, il faut préciser que la loi britannique est bien moins stricte que la nôtre sur l’utilisation des données médicales, ce qui n’est pas sans soulever des questions éthiques délicates. De plus, les pays anglo-saxons ont établi depuis des années des relations de synergie entre la recherche académique et la santé publique.
Du côté de la génétique, la France a été parmi les premiers pays à séquencer le génome du SARS-CoV-2, le virus qui cause le Covid-19, mais il y a ensuite eu un décrochage. Le projet Emergen2, coordonné par Santé publique France et l’ANRS-MIE3, a redressé la barre en termes de quantité de génomes produits, mais on reste loin des Britanniques en termes de qualité et d’exploitation des données. La France a également adopté une approche basée sur du criblage génétique : plutôt que de séquencer tout le génome du virus, le criblage ne détecte que quelques mutations spécifiques de variants. Cela permet de tester tous les échantillons positifs, ce qui serait bien trop long et coûteux avec le séquençage de génomes complets.
Notre équipe a ainsi pu rapidement alerter sur les vagues des variants Alpha, Delta ou Omicron. Cette exhaustivité et réactivité se paient en termes de spécificité et, par exemple, il est actuellement impossible de distinguer BA.1 de BA.2 en France avec le criblage.
Avant l’arrivée d’Omicron, certaines voix avaient émis l’espoir que le virus du Covid-19 ait déjà épuisé une grande partie de son potentiel évolutif. Comment est-ce que cela se mesure et où en sommes-nous vraiment ?
S. A. On a en effet retrouvé plusieurs mutations en commun dans différents variants. Le cas le plus frappant est celui de la mutation D614G, qui est apparue très vite et indépendamment dans différents pays. De tels cas d’évolution parallèle sont généralement le signe d’une forte pression de sélection.
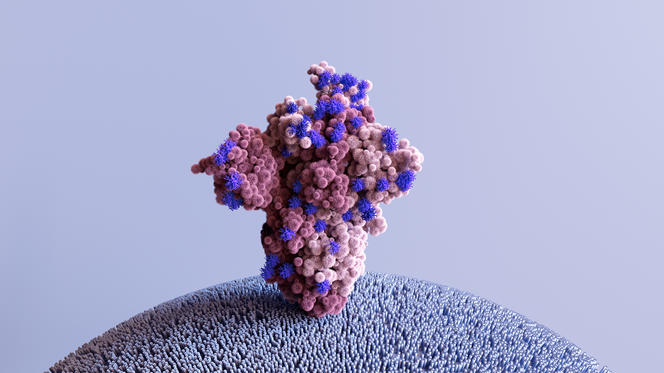
Mais le passage imposé par des mutations conférant un avantage sélectif ne présage pas forcément d’un resserrement des possibilités. Au contraire, une mutation peut ouvrir un nouveau paysage évolutif, comme cela semble avoir été le cas avec la mutation N501Y. À la décharge de l’hypothèse du rétrécissement évolutif, l’organisation des génomes viraux impose d’énormes contraintes en termes mutationnels. Quand notre ADN compte plusieurs milliards de paires de bases, le SARS-CoV-2 doit effectuer tout son cycle de vie avec 29 000 paires : s’introduire dans des organismes, puis dans leurs cellules, dupliquer son matériel génétique, produire des nouveaux virions, le tout en échappant à la réponse immunitaire. C’est pourquoi la majorité des mutations possibles ont un effet délétère sur le virus, certaines sont neutres, et seule une minorité peut être avantageuse.
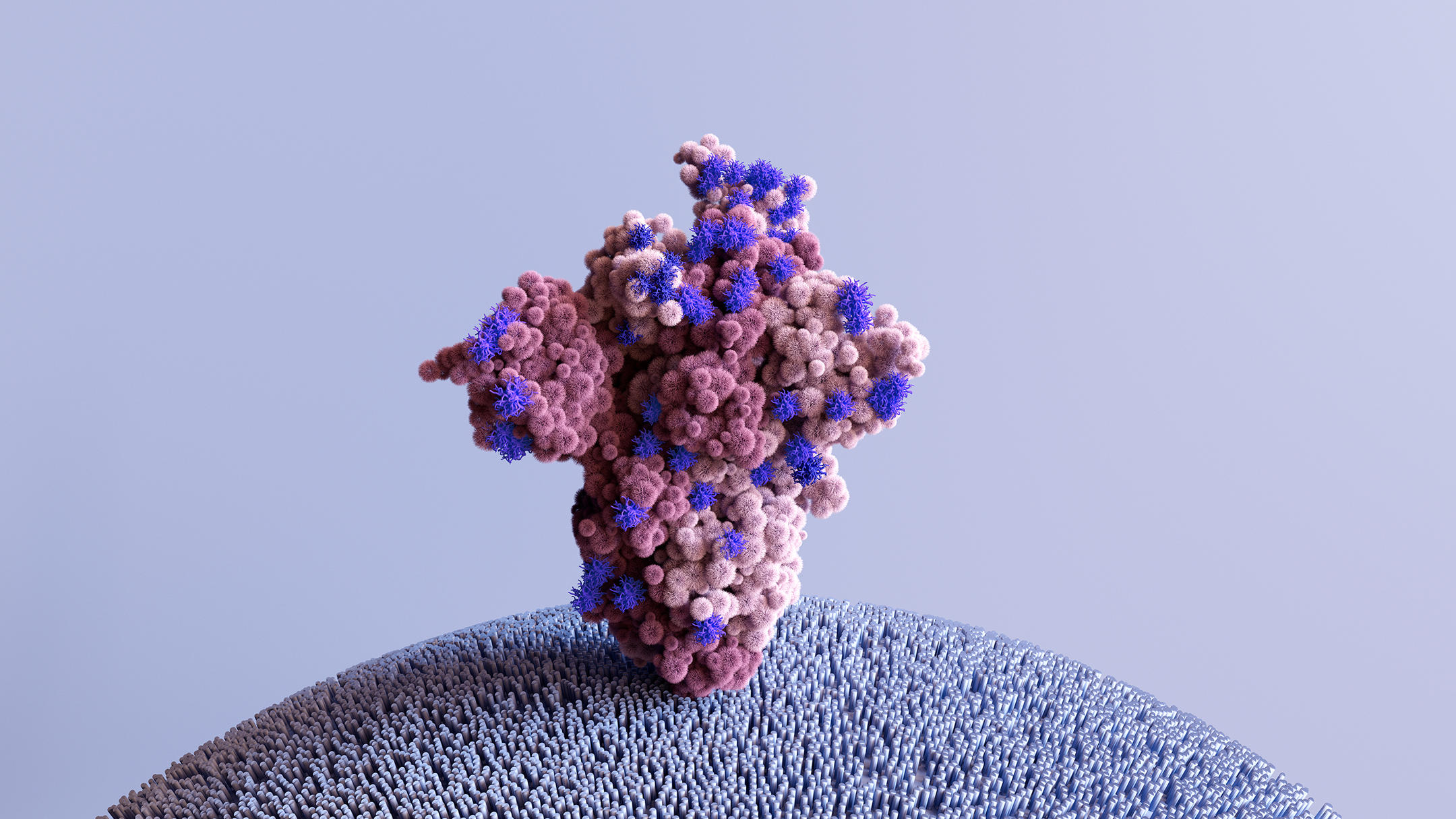
Les expériences de mutagenèse permettent de muter artificiellement certaines parties du virus afin d’étudier d’éventuels changements phénotypiques, c’est-à-dire de leurs propriétés. Bien entendu, cela se fait sur des fragments et des protéines isolés, et non sur un virus complet et viable. Les travaux existants portent principalement sur la protéine Spike, qui est à l’interface entre les particules virales et nos cellules. Des travaux, notamment ceux de l’équipe de Jesse Bloom, du laboratoire Fred Hutch4, ont ainsi identifié des mutations qui augmentent plusieurs centaines de fois l’affinité de cette protéine Spike pour le récepteur ACE2, qui sert de voie d’entrée du virus dans la cellule.
Mais si on peut anticiper les effets d’une mutation prise isolément, la dimension des combinaisons possibles rend l’opération quasiment impossible dès que l’on considère plusieurs mutations. Or, le variant Omicron diffère déjà de la lignée ancestrale de Wuhan par plus de cinquante mutations.
Existe-t-il des moyens de limiter ce potentiel de mutations, et donc l’émergence de variants inédits ?
S. A. Chaque fois que quelqu’un est contaminé, des milliards de nouvelles particules virales sont produites et accroissent, suite à des erreurs de copie, les risques d’émergence de mutants au hasard. Cet effet est renforcé lorsqu’une personne est infectée par plusieurs lignes différentes du fait de la recombinaison : si deux virus sont présents dans une même cellule, des échanges de portions entières de génomes peuvent avoir lieu. Encore une fois, mutations et recombinaisons ont de grandes chances d’être délétères pour le virus, mais certaines peuvent être problématiques pour nous. Et avec des tailles de population gigantesques, l’improbable peut devenir fréquent. Mais en résumé, plus la circulation du virus augmente, plus son évolution accélère. À ce sujet, les cas documentés de circulation du SARS-CoV-2 dans des réservoirs animaux, jusque dans les égouts de New York, sont inquiétants.

Enfin, pour comprendre l’évolution virale, il faut se pencher sur la dynamique intrahôte. Chez la majorité des personnes, l’infection dure moins de deux semaines et on estime qu’une nouvelle infection n’est établie que par un ou trois virions. Ce goulet d’étranglement limite fortement la diversification du virus. En quelque sorte, la diversité virale est pratiquement remise à zéro à chaque nouvelle infection. Toutefois, chez les personnes immunodéprimées, l’infection peut durer plusieurs mois, causant des pathologies lourdes. D’un point de vue évolutif, le processus n’est plus interrompu par les goulets d’étranglement hebdomadaires et la diversité virale croît au cours des mois. Ceci renforce la vitesse d’évolution puisque les mutations sont le moteur de la sélection naturelle. Ainsi, plusieurs études ont montré que certaines des lignées qui évoluent au sein d’infections de personnes immunodéprimées portent des mutations clés de certains variants. L’impératif de prévention et de suivi des personnes immunodéprimées est donc à la fois sanitaire, mais aussi évolutionnaire. Dans tous les cas, mettre en place des politiques de prévention afin de baisser au maximum le nombre de contaminations est le meilleur moyen de réduire les risques d’apparition de nouveaux variants de SARS-CoV-2. ♦
- 1. Directeur de recherche au CNRS, au Centre interdisciplinaire de recherche en biologie (CNRS/Collège de France/Inserm).
- 2. Consortium pour la surveillance et la recherche sur les infections à pathogènes émergents via la génomique microbienne.
- 3. Agence nationale de recherches sur le sida et les hépatites virales et les maladies infectieuses émergentes.
- 4. Centre de recherche contre le cancer Fred Hutchinson (Seattle, États-Unis).
Voir aussi
Auteur
Diplômé de l’École supérieure de journalisme de Lille, Martin Koppe a notamment travaillé pour les Dossiers d’archéologie, Science et Vie Junior et La Recherche, ainsi que pour le site Maxisciences.com. Il est également diplômé en histoire de l’art, en archéométrie et en épistémologie.