Vous êtes ici
Alzheimer : où en est la recherche?

Elle fait peur, évoque la perte de soi, la mort sociale… La maladie d’Alzheimer touche 5 % des plus de 65 ans, soit près d’un million de Français. Et « c’est sans compter les aidants ! Un malade est souvent entouré par deux ou trois proches », précise Martine Bungener, économiste et sociologue. Directrice de recherche émérite au CNRS, elle s’intéresse de près aux malades depuis des années.
Si elle n’a pas abouti à ce jour à un traitement, la recherche sur la maladie d’Alzheimer, de plus en plus médiatisée et financée, avance quant à elle à grands pas. Et depuis 2007, la définition même de la maladie a été totalement bouleversée, grâce à l’instauration d’un cadre précis pour l’identifier. « Un nouveau monde s’est offert à nous, on est sorti de la préhistoire », résume le neurologue Bruno Dubois, responsable du Centre des maladies cognitives et comportementales à l’hôpital de la Pitié-Salpêtrière, qui a grandement contribué à l'émergence de ces nouvelles définitions.
Des critères cliniques bien définis
Il y a encore une quinzaine d’années, le diagnostic d’Alzheimer se mêlait à celui d’autres démences. « On pensait que c’était une maladie très hétérogène, mais pas du tout ! » explique le neurologue. Désormais, les critères cliniques sont bien définis. Par exemple, la maladie atteint l’hippocampe dès le début, provoquant un syndrome amnésique qui s’étend ensuite au cortex cérébral.
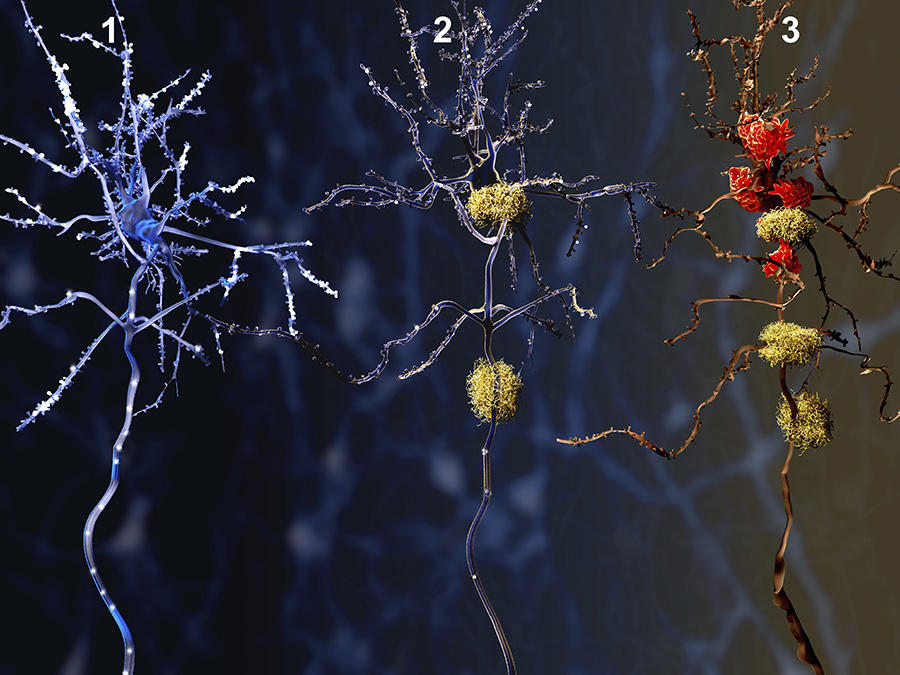
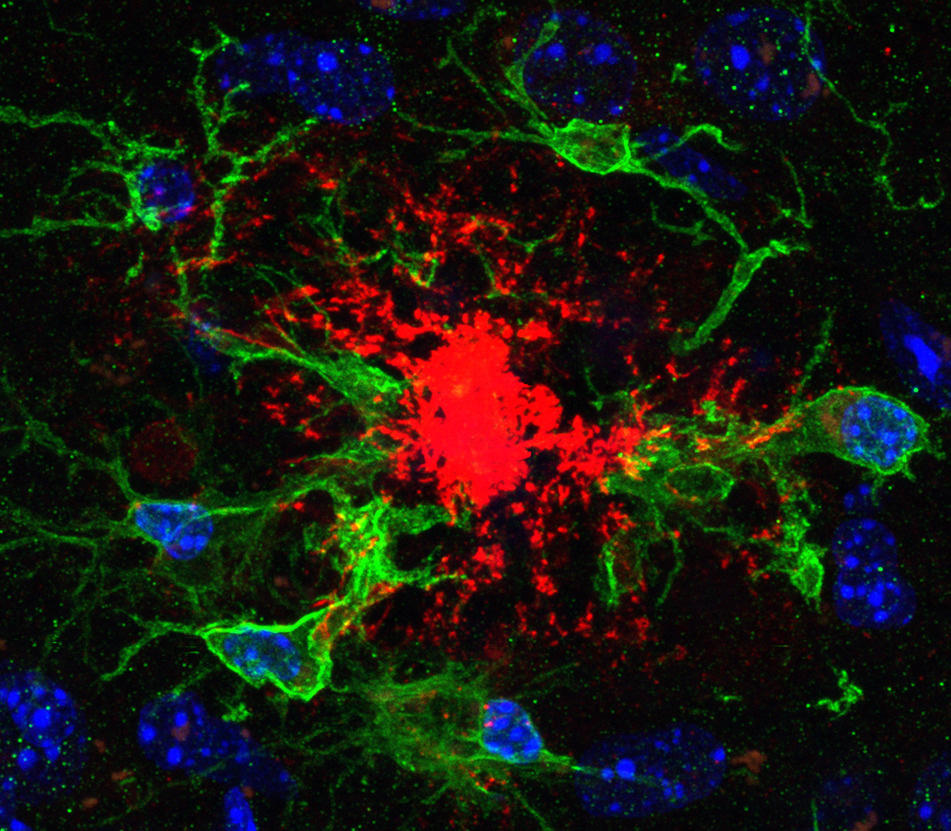
Dorénavant, Alzheimer est définie par trois lésions majeures : la perte neuronale, l’accumulation de peptides bêta-amyloïdes (qui forment les plaques amyloïdes) et enfin l’agrégation des protéines tau, qui engendrent une dégénérescence neurofibrillaire. « Ce cadre moderne change tout ! » s’enthousiasme Bruno Dubois, précisant qu’avant cela, les faux diagnostics pouvaient atteindre 35 %…
Depuis, de nombreuses recherches s’intéressent aux mécanismes aboutissant à cette maladie mise en lumière au début du XXe siècle par Alois Alzheimer. Ronald Melki, directeur de recherche à l’institut des neurosciences Paris-Saclay1, fait partie, lui aussi, de ceux qui ont permis d’y voir plus clair. En 2008, il a montré, avec son équipe, que des agrégats protéiques responsables de la dégénérescence pouvaient se transmettre d’une cellule à l’autre, « comme une infection », précise-t-il. « Au bout d’un certain moment, cette propagation accompagnée d’amplification atteint une grande partie du cerveau. En réalité, c’est quelque chose que l’on connaît très bien pour les maladies à prion, comme celle de la vache folle », indique-t-il. La maladie d’Alzheimer pourrait-elle dès lors être contagieuse ? « Pour l’instant, nous n’avons pas montré de transmission, il faudrait qu’il y ait un contact de cerveau à cerveau », estime le chercheur, ce qui paraît plus qu’improbable.

De plus, hormis pour les formes génétiques de la maladie, « il n’y a pas de surproduction des peptides amyloïdes, mais une baisse de leur dégradation due à une perte dépendante de l’âge », ajoute Frédéric Checler, directeur de recherche à l’Institut de pharmacologie moléculaire et cellulaire2 (IPMC), à Nice. L’âge intervient donc de manière directe dans la mort neuronale.
Les biomarqueurs, un « changement de paradigme »
Agrégat protéique, modification de l’hippocampe, perte neuronale… Ces signes, s’ils sont visibles, aident-ils à poser un diagnostic ? Oui, et les innovations en la matière ont connu un réel tournant ces cinq dernières années, notamment avec l’arrivée des tests biologiques. Auparavant, l’établissement du diagnostic se faisait grâce à un faisceau d’indices : IRM et tests cognitifs notamment. « On donnait des résultats au doigt mouillé. L’objectif était surtout d’éliminer les autres pathologies, et ensuite on estimait une probabilité que ce soit la maladie d’Alzheimer », raconte Bruno Dubois. Désormais, les médecins possèdent une preuve biologique du vivant des patients : les biomarqueurs, détectés grâce à une analyse du liquide céphalorachidien, recueilli par ponction lombaire. « Par exemple, chez une personne malade, on retrouve la protéine tau dans ce liquide à des taux anormalement élevés. Et à l’inverse, il devrait y avoir des peptides amyloïdes, mais on ne les observe pas en cas d’Alzheimer, car ils restent enfermés dans les plaques amyloïdes », détaille le neurobiologiste Luc Buée, directeur de recherche au centre de recherche Jean-Pierre-Aubert, à Lille.
Autre avantage des biomarqueurs, et pas des moindres : ils sont détectables à n’importe quel stade de la maladie, même lorsqu’elle est encore silencieuse. « C’est un changement total de paradigme », assure Bruno Dubois. Seulement, détecter Alzheimer alors que les pertes de mémoire ou la confusion ne sont pas encore installées pose de réels problèmes éthiques, car aucun traitement curatif ne pourra être proposé au malade. « Les biomarqueurs doivent rester un complément diagnostique, lorsqu’il y a un doute, ou chez des personnes jeunes par exemple », prévient le neurologue.

Des facteurs de risque mieux connus
Sans traitement, et malgré les progrès de la recherche, le diagnostic de la maladie tombe toujours comme un couperet. Martine Bungener raconte que ce douloureux moment est souvent vécu « comme une annonce de mort sociale, comme si tout le regard de la société pesait sur le patient ». Et les premières interrogations des malades ne sont pas tournées vers la médecine ou la science, mais bien vers les difficultés de la vie quotidienne à venir. « Les patients ont l’impression qu’ils vont bientôt devenir quelqu’un qui n’existe pas, mais ils n’ont pas envie qu’on les stigmatise, ce qu’ils veulent c’est une liberté de choix de vie, encore », insiste la sociologue. Ainsi, certains poussent leur proche malade à continuer de cuisiner, de lire, voire de conduire !
« Pourquoi moi ? » Voici l’une des questions qui reviennent le plus souvent à l’annonce du diagnostic, rapporte Martine Bungener. Dans certains cas, les facteurs de risque sont bien identifiés, comme la forme génétique. « Il existe des mutations génétiques très rares qui provoquent la maladie, mais ces patients ne représentent que 0,3 % des formes d’Alzheimer. Ces mutations sont portées par des gènes impliqués dans la genèse des peptides amyloïdes », indique Luc Buée. Par ailleurs, une mauvaise hygiène de vie, et les pathologies qui y sont associées, comme le diabète ou l’hypertension, « conduit à une fragilisation du cerveau favorisant la maladie », ajoute-t-il.
Plus curieusement, la recherche a récemment montré que « des symptômes très proches d’Alzheimer se développaient chez des boxeurs, des joueurs de football américain ou encore de hockey », relève le chercheur.
Le facteur de risque le mieux identifié reste néanmoins l’âge. « Avec le temps, les protéines vont s’agréger dans le cerveau. Et plus la vie dure longtemps, plus la probabilité d’accumulation des protéines augmente », rappelle Ronald Melki. D’autres pistes explicatives ont été explorées, comme l’infection bactérienne ou virale, mais elles restent aujourd’hui peu concluantes. « L’un des meilleurs moyens de prévention est de faire fonctionner son cerveau, avec de la lecture ou des discussions. À cela il faut ajouter un exercice physique régulier et constant, qui va oxygéner le cerveau et lui apporter des nutriments », conseille le spécialiste.
Des pistes thérapeutiques à la peine
Mieux connaître les facteurs de risque et les lésions d’Alzheimer pourrait permettre d’interférer sur ces mécanismes et de développer un traitement efficace. Beaucoup de molécules et de stratégies thérapeutiques ont été testées ces dernières années, à commencer par l’immunothérapie. L’idée paraît simple : créer des anticorps qui iront cibler le peptide amyloïde et ainsi détruire les plaques. « C’est ce que l’on a appelé le vaccin », indique Luc Buée. Une stratégie qui s’est révélée décevante car elle ne ralentissait pas la dégénérescence, malgré une chute effective de la présence des plaques dans le cerveau. « Cibler les plaques et s’en servir d’indicateur de succès lors d’essais cliniques explique peut-être la somme considérable d’échecs », avance Frédéric Checler.
Deuxième stratégie : intervenir plus en amont, avant la formation des plaques, pour empêcher leur développement. Ainsi, « la connaissance en matière de maturation de précurseur des peptides amyloïdes révèle de nouveaux acteurs », explique Frédéric Checler. Une enzyme est particulièrement ciblée : la bêta-sécrétase, qui participe à la formation des peptides amyloïdes. En bloquant cette enzyme grâce à un inhibiteur, la cascade de réactions entraînant la maladie serait stoppée. « Chez l’homme, on a montré que ça inhibait l’enzyme à 70 % », précise Bruno Dubois. Frédéric Checler se veut optimiste : « Seule cette compréhension des mécanismes impliqués, et de leurs dysfonctions, permettra d’identifier des pistes pharmacologiques visant à bloquer le développement de la pathologie ou, tout au moins, d’interférer dans sa progression », estime-t-il.

Enfin, la dernière manœuvre à l’essai consiste à éviter l’agrégation de tau, en utilisant une molécule qui stabiliserait la protéine et l’empêcherait d’entraîner des dégénérescences neurofibrillaires. « Pour cela, on s’intéresse beaucoup aux polyphénols par exemple, présents dans le thé vert, le curcuma ou même le vin », indique Ronald Melki. Si cette piste est exploitée à fond par l’industrie, les polyphénols restent difficilement métabolisables par le foie.
Mieux accompagner les patients
Pour l’instant, la majorité des pistes thérapeutiques curatives restent décevantes. « Beaucoup d’efforts et d’espoirs ont été mis sur l’immunothérapie notamment, avec quatre ou cinq molécules prometteuses, qui n’ont finalement pas été assez efficaces. Nous sommes très déçus pour les patients », reconnaît Bruno Dubois. « Ça fait presque 20 ans que l’on cherche à trouver une bonne combinaison, signale Ronald Melki. Dans 10 ou 15 ans, nous aurons sûrement beaucoup plus de solutions ». « La maladie d’Alzheimer sera, si ce n’est vaincue, tout au moins contrôlée dans son évolution », espère pour sa part Frédéric Checler.
Et si la réponse se trouvait finalement aussi dans la vie quotidienne des patients ? La stimulation leur permet en effet de garder une certaine autonomie. « Les proches et les malades font preuve d’une inventivité extraordinaire, c’est fascinant ! », s’enthousiasme Martine Bungener, qui relève que les aidants « ne veulent pas retirer ce qui a été important auparavant pour le malade, comme faire encore la cuisine. Et ça marche ! Les malades sont plus calmes, moins agressifs ». L’image dramatique de la maladie s’efface peu à peu… « Il faut comprendre que les gestes vont être lents, mais que ce n’est pas grave », renchérit-elle. Et le corps médical est en progrès constant pour améliorer l’annonce du diagnostic et l’accompagnement des patients. « Tout l’objectif est d’accompagner, sans perdre de vue la vie d'avant », résume ainsi la chercheuse.
Lire aussi : « Alzheimer : les espoirs de la piste sanguine » et « La musique pour soigner la mémoire »
Voir aussi
Auteur
Léa Galanopoulo est journaliste scientifique, spécialisée en santé, médecine et biologie.